Тема: Основные симптомы и синдромы заболеваний органов дыхания. Исследование дыхательной системы. Основые клинические синдромы при заболеваниях органов дыхания
ОСНОВНЫЕ СИМПТОМЫ И СИНДРОМЫ ПРИ ЗАБОЛЕВАНИЯХ ОРГАНОВ ДЫХАНИЯ Часть1 Расспрос больных с заболеваниями органов дыхания. Осмотр и пальпация грудной клетки. Сравнительная и топографическая перкуссия легких

 ЖАЛОБЫ Боль, кашель, кровохарканье, одышка, Боль (dolor) в грудной клетке может быть обусловлена поражением элементов системы дыхания: плевры, ребер, межреберных мышц, нервов и т. д. , а также других систем, например сердечно-сосудистой, опорно-двигательной. Боль должна быть детализована: необходимо указать локализацию, характер, интенсивность, продолжительность, условия возникновения и купирование боли.
ЖАЛОБЫ Боль, кашель, кровохарканье, одышка, Боль (dolor) в грудной клетке может быть обусловлена поражением элементов системы дыхания: плевры, ребер, межреберных мышц, нервов и т. д. , а также других систем, например сердечно-сосудистой, опорно-двигательной. Боль должна быть детализована: необходимо указать локализацию, характер, интенсивность, продолжительность, условия возникновения и купирование боли.
 При заболевании трахеи и бронхов боль локализуется за грудиной, носит характер саднения, жжения, неинтенсивная, усиливается или появляется при кашле и не изменяется при дыхании. Мышечные боли в следствие значительного надсадного кашля локализуются в нижнебоковых отделах грудной клетки, имеют тянущий, колющий характер, различной интенсивности, не иррадиируют, появляются приступах кашля, не усиливаются при медленном глубоком вдохе.
При заболевании трахеи и бронхов боль локализуется за грудиной, носит характер саднения, жжения, неинтенсивная, усиливается или появляется при кашле и не изменяется при дыхании. Мышечные боли в следствие значительного надсадного кашля локализуются в нижнебоковых отделах грудной клетки, имеют тянущий, колющий характер, различной интенсивности, не иррадиируют, появляются приступах кашля, не усиливаются при медленном глубоком вдохе.
 Плевральные боли имеют локализованный характер, не иррадиируют, колющего характера выраженной интенсивности, резко усиливаются при дыхании, особенно при сгибании больного в здоровую сторону. Боли, обусловленные межреберной невралгией, также локализованы, иррадиируют в спину, колющие, выраженной интенсивности, усиливаются при глубоком дыхании, поворотах туловища, при сгибании пациента в больную сторону.
Плевральные боли имеют локализованный характер, не иррадиируют, колющего характера выраженной интенсивности, резко усиливаются при дыхании, особенно при сгибании больного в здоровую сторону. Боли, обусловленные межреберной невралгией, также локализованы, иррадиируют в спину, колющие, выраженной интенсивности, усиливаются при глубоком дыхании, поворотах туловища, при сгибании пациента в больную сторону.
 Кашель (tussis) – сложнорефлекторный акт защиты и самоочищения дыхательных путей в ответ на раздражение рецепторов глотки, гортани, трахеи, долевых и сегментарных бронхов, плевры. Кашлем не сопровождается патологический процесс, локализующийся только в паренхиме легких или в мелких бронхах, пока мокрота не попадет в крупные бронхи. Появление кашля возможно при раздражении рецепторов блуждающего нерва, расположенных в других органах (опухоль средостения, аневризма аорты, увеличение левого предсердия и др.) Сухой (непродуктивный) кашель, без отделения мокроты наблюдается в начальной стадии воспаления слизистой бронхов и легких, при наличии очень вязкой мокроты и при поражении плевры, средостения, у ослабленных больных. Продуктивный кашель характеризуется отделением мокроты после 2 -3 кашлевых толчков, сила которых сохранена. При кашле отсутствуют признаки усиления дыхательной недостаточности (усиление одышки и цианоза), сопровождается отделением мокроты. Малопродуктивный кашель характеризуется продолжительными признаками мучительного надсадного кашля с большим количеством кашлевых толчков, часто сопровождается признаками усиления дыхательной недостаточности обструктивного типа (одышки, цианоза, набухании шейных вен и т. п.), сопровождается отделением некоторого количества мокроты. Обычно встречается при обструктивном бронхите и бронхиальной астме.
Кашель (tussis) – сложнорефлекторный акт защиты и самоочищения дыхательных путей в ответ на раздражение рецепторов глотки, гортани, трахеи, долевых и сегментарных бронхов, плевры. Кашлем не сопровождается патологический процесс, локализующийся только в паренхиме легких или в мелких бронхах, пока мокрота не попадет в крупные бронхи. Появление кашля возможно при раздражении рецепторов блуждающего нерва, расположенных в других органах (опухоль средостения, аневризма аорты, увеличение левого предсердия и др.) Сухой (непродуктивный) кашель, без отделения мокроты наблюдается в начальной стадии воспаления слизистой бронхов и легких, при наличии очень вязкой мокроты и при поражении плевры, средостения, у ослабленных больных. Продуктивный кашель характеризуется отделением мокроты после 2 -3 кашлевых толчков, сила которых сохранена. При кашле отсутствуют признаки усиления дыхательной недостаточности (усиление одышки и цианоза), сопровождается отделением мокроты. Малопродуктивный кашель характеризуется продолжительными признаками мучительного надсадного кашля с большим количеством кашлевых толчков, часто сопровождается признаками усиления дыхательной недостаточности обструктивного типа (одышки, цианоза, набухании шейных вен и т. п.), сопровождается отделением некоторого количества мокроты. Обычно встречается при обструктивном бронхите и бронхиальной астме.
 При описании кашля с мокротой необходимо указать количество мокроты, ее цвет, запах, в каком положении легче отходит, наличие включений в мокроту. Различают: слизистую вязкую мокроту беловатого цвета, которая характерна для начальной стадии воспаления слизистой бронхов или легочной паренхимы); слизисто-гнойную мокроту беловатого цвета или сероватозеленого, которая характерна для большинства воспалительных заболеваний легких и бронхов; серозную жидкую мокроту, которая при наличии примеси крови может иметь розовый цвет. Обычно наблюдается при отеке легких, часто имеет пенистый вид; гнойную мокроту, которая имеет вязкий, зеленоватый цвет, нередко неприятных запах, при стоянии образует три или два слоя. Гнойные мокроты характерны для острых и хронических гнойных заболеваний (абсцесс легких, бронхоэктаз, гангрена легких).
При описании кашля с мокротой необходимо указать количество мокроты, ее цвет, запах, в каком положении легче отходит, наличие включений в мокроту. Различают: слизистую вязкую мокроту беловатого цвета, которая характерна для начальной стадии воспаления слизистой бронхов или легочной паренхимы); слизисто-гнойную мокроту беловатого цвета или сероватозеленого, которая характерна для большинства воспалительных заболеваний легких и бронхов; серозную жидкую мокроту, которая при наличии примеси крови может иметь розовый цвет. Обычно наблюдается при отеке легких, часто имеет пенистый вид; гнойную мокроту, которая имеет вязкий, зеленоватый цвет, нередко неприятных запах, при стоянии образует три или два слоя. Гнойные мокроты характерны для острых и хронических гнойных заболеваний (абсцесс легких, бронхоэктаз, гангрена легких).
 Кровохарканье (haemoptoe)- наличие крови в мокроте. Может быть в виде едва заметных прожилок, алой, пенистой крови, темных кровянистых сгустков или мокроты «ржавого» цвета за счет распада эритроцитов и образования пигмента гемосидерина. Кровохарканье встречается при раке и туберкулезе легкого, пневмонии, абсцессе и гангрене легкого, бронхоэктатической болезни, трахеите, ларингите, тромбоэмболии легочной артерии.
Кровохарканье (haemoptoe)- наличие крови в мокроте. Может быть в виде едва заметных прожилок, алой, пенистой крови, темных кровянистых сгустков или мокроты «ржавого» цвета за счет распада эритроцитов и образования пигмента гемосидерина. Кровохарканье встречается при раке и туберкулезе легкого, пневмонии, абсцессе и гангрене легкого, бронхоэктатической болезни, трахеите, ларингите, тромбоэмболии легочной артерии.
 Одышка (duspnoe) – субъективное ощущение нехватки воздуха, сопровождающиеся изменением глубины и ритма дыхательных движений. Основной причиной одышки является раздражение дыхательного центра гиперкапнией, рефлекторным, токсическим и другими воздействиями. Варианты одышки: - Инспираторная одышка с признаками затруднения вдоха. Встречается при сдавливании легкого и ограничении экскурсии легких (гидроторакс, пневмоторакс, фиброторакс, паралич дыхательных мышц, выраженная деформация грудной клетки и т. д.), а также патологических процессах в легких, сопровождающихся уменьшением легочной ткани (воспалительный или гемодинамический отек), неврозах, сопровождающихся спазмом дыхательной мускулатуры. -Экспираторная одышка с затруднением вдоха чаще всего свидетельствует о наличии бронхиальной обструкции. В механизме возникновения отдышки важное значение имеет раннее экспираторное закрытие бронхов (коллапс бронхов) вследствие разности давления в грудной клетке при вдохе и выдохе, а также слабости бронхиальной стенки при врожденных состояниях (проллапс бронхиол). Кроме того, экспираторной одышке способствует и феномен Бертуали – уменьшение давления в узких бронхиолах за счет увеличения скорости прохождения потока воздуха. -Смешанная одышка с затруднением выдоха и вдоха, встречается при патологических процессах, сопровождающихся нарушениями, приводящими как к инспираторной, так и экспираторной одышке. Например, фиброз легочной ткани на фоне хронического обструктивного бронхита и эмфиземе легких, силикоз легких и обструктивный бронхит и т. д. -Частое дыхание, вплоть до гипервентиляционного синдрома. Больные не могут четко определить, затруднен вдох или выдох, субъективно ощущают нехватку воздуха. Встречается при психоэмоциональном напряжении, неврозах, при лихорадке, анемии, отеке легких. -Стридорозное дыхание возникает при механическом препятствии в верхних дыхательных путях. Затрудняется вдох и выдох, дыхание становится шумным, громким, слышным на расстоянии. -Брадипноэ - патологическое урежение дыхания, наблюдается при кровоизлияниях в головной мозг, тяжелой гипоксии, тяжелых интоксикациях, инфекционных процессах.
Одышка (duspnoe) – субъективное ощущение нехватки воздуха, сопровождающиеся изменением глубины и ритма дыхательных движений. Основной причиной одышки является раздражение дыхательного центра гиперкапнией, рефлекторным, токсическим и другими воздействиями. Варианты одышки: - Инспираторная одышка с признаками затруднения вдоха. Встречается при сдавливании легкого и ограничении экскурсии легких (гидроторакс, пневмоторакс, фиброторакс, паралич дыхательных мышц, выраженная деформация грудной клетки и т. д.), а также патологических процессах в легких, сопровождающихся уменьшением легочной ткани (воспалительный или гемодинамический отек), неврозах, сопровождающихся спазмом дыхательной мускулатуры. -Экспираторная одышка с затруднением вдоха чаще всего свидетельствует о наличии бронхиальной обструкции. В механизме возникновения отдышки важное значение имеет раннее экспираторное закрытие бронхов (коллапс бронхов) вследствие разности давления в грудной клетке при вдохе и выдохе, а также слабости бронхиальной стенки при врожденных состояниях (проллапс бронхиол). Кроме того, экспираторной одышке способствует и феномен Бертуали – уменьшение давления в узких бронхиолах за счет увеличения скорости прохождения потока воздуха. -Смешанная одышка с затруднением выдоха и вдоха, встречается при патологических процессах, сопровождающихся нарушениями, приводящими как к инспираторной, так и экспираторной одышке. Например, фиброз легочной ткани на фоне хронического обструктивного бронхита и эмфиземе легких, силикоз легких и обструктивный бронхит и т. д. -Частое дыхание, вплоть до гипервентиляционного синдрома. Больные не могут четко определить, затруднен вдох или выдох, субъективно ощущают нехватку воздуха. Встречается при психоэмоциональном напряжении, неврозах, при лихорадке, анемии, отеке легких. -Стридорозное дыхание возникает при механическом препятствии в верхних дыхательных путях. Затрудняется вдох и выдох, дыхание становится шумным, громким, слышным на расстоянии. -Брадипноэ - патологическое урежение дыхания, наблюдается при кровоизлияниях в головной мозг, тяжелой гипоксии, тяжелых интоксикациях, инфекционных процессах.
 Патологические типы дыхания 1. Дыхание Грокка – периодически поверхносное дыхание сменяется глубоким 2. Дыхание Чейн-Стокса – периоды апноэ с последующим нарастанием глубины дыхания. 3. Дыхание Биота – периоды апноэ с последующим восстановлением ритма дыхания, Наблюдаются при отеке мозга, инсульте, менингитах, энцефалитах. 4. Дыхание Куссмауля глубокое, относительно ровное, шумное дыхание, часто у больных с токсическим поражением дыхательного центра Наблюдается при диабетической, уремической, печеночной коме. Брадипноэ - патологическое урежение дыхания, наблюдается при кровоизлияниях в головной мозг, тяжелой гипоксии, тяжелых интоксикациях, инфекционных процессах. Удушье (asthma) – внезапно наступающие выраженное чувство нехватки воздуха, сопровождающие и признаками дыхательной недостаточности. Следует обращать внимание на соотношение частоты дыхания и пульса. В норме составляет 1: 4. В норме частота дыхания в покое составляет 12 -18 движений в минуту.
Патологические типы дыхания 1. Дыхание Грокка – периодически поверхносное дыхание сменяется глубоким 2. Дыхание Чейн-Стокса – периоды апноэ с последующим нарастанием глубины дыхания. 3. Дыхание Биота – периоды апноэ с последующим восстановлением ритма дыхания, Наблюдаются при отеке мозга, инсульте, менингитах, энцефалитах. 4. Дыхание Куссмауля глубокое, относительно ровное, шумное дыхание, часто у больных с токсическим поражением дыхательного центра Наблюдается при диабетической, уремической, печеночной коме. Брадипноэ - патологическое урежение дыхания, наблюдается при кровоизлияниях в головной мозг, тяжелой гипоксии, тяжелых интоксикациях, инфекционных процессах. Удушье (asthma) – внезапно наступающие выраженное чувство нехватки воздуха, сопровождающие и признаками дыхательной недостаточности. Следует обращать внимание на соотношение частоты дыхания и пульса. В норме составляет 1: 4. В норме частота дыхания в покое составляет 12 -18 движений в минуту.
 Положение тела у больных с заболеваниями системы дыхания: лежа на одном боку (на пораженной стороне при массивном плевральном выпоте, воспалении легких, сухом плеврите); сидя на кровати, упираясь руками в ее край (при обструктивных состояниях), что облегчает экскурсию грудной клетки. У больных с заболеваниями системы дыхания нередко наблюдается диффузный (центральный, теплый) цианоз. Однако следует помнить, что цианоз не выявляется у пациентов с анемией (гемоглобин менее 80 г/л). Часто обнаруживается набухание шейных вен у больных с эмфиземой легких, которое обусловлено повышением внутригрудного давления.
Положение тела у больных с заболеваниями системы дыхания: лежа на одном боку (на пораженной стороне при массивном плевральном выпоте, воспалении легких, сухом плеврите); сидя на кровати, упираясь руками в ее край (при обструктивных состояниях), что облегчает экскурсию грудной клетки. У больных с заболеваниями системы дыхания нередко наблюдается диффузный (центральный, теплый) цианоз. Однако следует помнить, что цианоз не выявляется у пациентов с анемией (гемоглобин менее 80 г/л). Часто обнаруживается набухание шейных вен у больных с эмфиземой легких, которое обусловлено повышением внутригрудного давления.
 Определение формы грудной клетки Для определение формы грудной клетки необходимо исследовать: 1. Размеры грудной клетки (переднезадний и боковой); 2. Над- и подключичные ямки; 3. Угол соединения тела и рукоятки грудины; 4. Эпигастральный (надчревный) угол; 5. Направление ребер в боковых отделах грудной клетки; 6. Межреберные промежутки; 7. Прилегание лопаток к грудной клетки.
Определение формы грудной клетки Для определение формы грудной клетки необходимо исследовать: 1. Размеры грудной клетки (переднезадний и боковой); 2. Над- и подключичные ямки; 3. Угол соединения тела и рукоятки грудины; 4. Эпигастральный (надчревный) угол; 5. Направление ребер в боковых отделах грудной клетки; 6. Межреберные промежутки; 7. Прилегание лопаток к грудной клетки.
 Формы грудной клетки у здорового человека Нормостеническая -отношение переднезаднего размера к поперечному 0, 65 -0, 75; -над и подключичные ямки обозначены слабо; -угол Людовика отчетливо выражен, -эпигастральный угол приближается к 90; -ребра в боковых отделах имеют умеренно косое направление; -лопатки плотно прилегают к грудной клетке и располагаются на одном уровне; -грудной отдел туловища по своей высоте примерно равен брюшному).
Формы грудной клетки у здорового человека Нормостеническая -отношение переднезаднего размера к поперечному 0, 65 -0, 75; -над и подключичные ямки обозначены слабо; -угол Людовика отчетливо выражен, -эпигастральный угол приближается к 90; -ребра в боковых отделах имеют умеренно косое направление; -лопатки плотно прилегают к грудной клетке и располагаются на одном уровне; -грудной отдел туловища по своей высоте примерно равен брюшному).
 Гиперстеническая -переднезадний размер приблежается к боковому; -отношение переднезаднего размера к поперечному больше 0, 75; -над и подключичные ямки не видны, «сглажены» ; -угол Людовика выражен значительно, -эпигастральный угол больше 90; -ребра имеют почти горизонтальное направление; -межреберные промежутки узкие; -лопатки плотно прилегают к задней поверхности грудной клетки; -поперечные размеры грудной клетки преобладают над продольными).
Гиперстеническая -переднезадний размер приблежается к боковому; -отношение переднезаднего размера к поперечному больше 0, 75; -над и подключичные ямки не видны, «сглажены» ; -угол Людовика выражен значительно, -эпигастральный угол больше 90; -ребра имеют почти горизонтальное направление; -межреберные промежутки узкие; -лопатки плотно прилегают к задней поверхности грудной клетки; -поперечные размеры грудной клетки преобладают над продольными).
 Астеническая -боковой размер преобладает над переднезадним; отношение переднезаднего размера к боковому меньше 0, 65; -над и подключичные ямки резко выделяются; -ребра имеют косое направление и приближаются к вертикальному; -угол соединения грудины с рукояткой (угол Людовика) отсутствует; -эпигастральный угол меньше 90; -межреберные промежутки расширены; -лопатки крыловидно отстают от грудной клетки; -продольный размер грудной клетки преобладают над поперечным).
Астеническая -боковой размер преобладает над переднезадним; отношение переднезаднего размера к боковому меньше 0, 65; -над и подключичные ямки резко выделяются; -ребра имеют косое направление и приближаются к вертикальному; -угол соединения грудины с рукояткой (угол Людовика) отсутствует; -эпигастральный угол меньше 90; -межреберные промежутки расширены; -лопатки крыловидно отстают от грудной клетки; -продольный размер грудной клетки преобладают над поперечным).
 патологические формы грудной клетки Эмфизематозная (бочкообразная) -переднезадний размер равен боковому; -ребра расположены горизонтально; -над и подключичные ямки сглажены; в их области наблюдается выбухание мягких тканей; -межреберные промежутки расширены; -эпигастральный угол тупой; -грудная клетка застыла на высоте вдоха. Встречается у больных с ХОБЛ и бронхиальной астмой.
патологические формы грудной клетки Эмфизематозная (бочкообразная) -переднезадний размер равен боковому; -ребра расположены горизонтально; -над и подключичные ямки сглажены; в их области наблюдается выбухание мягких тканей; -межреберные промежутки расширены; -эпигастральный угол тупой; -грудная клетка застыла на высоте вдоха. Встречается у больных с ХОБЛ и бронхиальной астмой.
 Паралитическая грудная клетка -плоская и узкая, переднезадний размер значительно уменьшен. -резко обрисовываются ключицы, которые обычно расположены ассиметрично, над и подключичные ямки резко и неодинаково западают, -лопатки резко отстают от грудной клетки, они расположены на разных уровнях и во время дыхания смещаются неодновременно (слабость мышц спины). -ребра расположены косо вниз, -эпигастральный угол острый (иногда 45), межреберные промежутки расширены. Встречается у больных с тяжелыми хроническими заболеваниями легких, сильно истощенных людей, при слабом конституциональном развитии.
Паралитическая грудная клетка -плоская и узкая, переднезадний размер значительно уменьшен. -резко обрисовываются ключицы, которые обычно расположены ассиметрично, над и подключичные ямки резко и неодинаково западают, -лопатки резко отстают от грудной клетки, они расположены на разных уровнях и во время дыхания смещаются неодновременно (слабость мышц спины). -ребра расположены косо вниз, -эпигастральный угол острый (иногда 45), межреберные промежутки расширены. Встречается у больных с тяжелыми хроническими заболеваниями легких, сильно истощенных людей, при слабом конституциональном развитии.
 Рахитическая (килевидная, куриная) -она является следствием деформации костей грудной клетки после перенесенного в детском возрасте рахита. -грудина выступает вперед в виде киля. -реберные хрящи на месте перехода их в кость четкообразно утолщаются («рахитические четки»).
Рахитическая (килевидная, куриная) -она является следствием деформации костей грудной клетки после перенесенного в детском возрасте рахита. -грудина выступает вперед в виде киля. -реберные хрящи на месте перехода их в кость четкообразно утолщаются («рахитические четки»).
 Воронкообразная -встречается как аномалия развития и характеризуется наличием в нижней трети грудины углубления, похожего на воронку. Ладьевидная -Характеризуется наличием продолговатого углубления середины верхней трети грудины, которая по форме напоминает углубление лодки. Встречается у лиц с заболеваниями спинного мозга (сирингомиелия).
Воронкообразная -встречается как аномалия развития и характеризуется наличием в нижней трети грудины углубления, похожего на воронку. Ладьевидная -Характеризуется наличием продолговатого углубления середины верхней трети грудины, которая по форме напоминает углубление лодки. Встречается у лиц с заболеваниями спинного мозга (сирингомиелия).

 Определение симметричности правой и левой половин грудной клетки и их участия в акте дыхания В норме обе половины грудной клетки имеют почти одинаковые размеры и одинаково участвуют в акте дыхания. Для придания синхронности движения правой и левой половин грудной клетки пациенту предлагают глубоко дышать и следить за углами лопаток, можно при этом накладывать руки таким образом, чтобы концевые фаланги больших пальцев находились у углов лопаток. Для оценки подвижности грудной клетки измеряют ее окружность в положении вдоха и выдоха. При спокойном дыхании эта разница (экскурсия грудной клетки) не превышает 2 -3 см. Максимальная экскурсия колеблется от 7, 0 до 8, 5 см. Уменьшение объема (западение) одной половины грудной клетки свидетельствует о сморщивании за ее стенкой органов легких и плевры (ателектаз, пневмосклероз, резекция легкого). Отставание одной половины грудной клетки в дыхании наблюдается при пневмониях, абсцессах легкого, обтурационном ателектазе, сморщивании легкого; патологических процессах в плевральной полости (экссудативный плеврит, гидроторакс, пневмоторакс, фиброторакс); сухом плеврите, межреберной невралгии, переломах ребер.
Определение симметричности правой и левой половин грудной клетки и их участия в акте дыхания В норме обе половины грудной клетки имеют почти одинаковые размеры и одинаково участвуют в акте дыхания. Для придания синхронности движения правой и левой половин грудной клетки пациенту предлагают глубоко дышать и следить за углами лопаток, можно при этом накладывать руки таким образом, чтобы концевые фаланги больших пальцев находились у углов лопаток. Для оценки подвижности грудной клетки измеряют ее окружность в положении вдоха и выдоха. При спокойном дыхании эта разница (экскурсия грудной клетки) не превышает 2 -3 см. Максимальная экскурсия колеблется от 7, 0 до 8, 5 см. Уменьшение объема (западение) одной половины грудной клетки свидетельствует о сморщивании за ее стенкой органов легких и плевры (ателектаз, пневмосклероз, резекция легкого). Отставание одной половины грудной клетки в дыхании наблюдается при пневмониях, абсцессах легкого, обтурационном ателектазе, сморщивании легкого; патологических процессах в плевральной полости (экссудативный плеврит, гидроторакс, пневмоторакс, фиброторакс); сухом плеврите, межреберной невралгии, переломах ребер.
 Пальпация грудной клетки Пальпация позволяет: Уточнить данные осмотра, касающиеся формы грудной клетки и характера дыхания; При наличии болезненности грудной клетки установить ее место и степень выраженности; Определить резистентность (эластичность) грудной клетки; Определить феномен голосового дрожания; При поражении плевры обнаружить шум трения плевры и шум плеска жидкости.
Пальпация грудной клетки Пальпация позволяет: Уточнить данные осмотра, касающиеся формы грудной клетки и характера дыхания; При наличии болезненности грудной клетки установить ее место и степень выраженности; Определить резистентность (эластичность) грудной клетки; Определить феномен голосового дрожания; При поражении плевры обнаружить шум трения плевры и шум плеска жидкости.
 Феномен голосового дрожания Пальпаторное ощущение вибрации грудной клетки пациента при произнесение слов, содержащих букву «р» . Голосовое дрожание изучается на симметричных участках грудной клетки, начиная сверху спереди. При этом оценивается степень вибрации грудной клетки справа и слева. При патологических процессах в легких или плевре голосовое дрожание может быть ослаблено (а иногда даже отсутствует) или наоборот усилено. Усиление голосового дрожания наблюдается при уплотнении легочной ткани хорошо проводящей звук (воспаление, инфаркт, туберкулез, ателектаз) или при наличии в легких полости, сообщающейся с бронхами (каверна, абсцесс, бронхоэктазы). Ослабление голосового дрожания может наблюдаться у тучных лиц, при эмфиземе легких, закупорке проводящего бронха, инородным телом, пневмотораксе, гидротораксе, фибротораксе.
Феномен голосового дрожания Пальпаторное ощущение вибрации грудной клетки пациента при произнесение слов, содержащих букву «р» . Голосовое дрожание изучается на симметричных участках грудной клетки, начиная сверху спереди. При этом оценивается степень вибрации грудной клетки справа и слева. При патологических процессах в легких или плевре голосовое дрожание может быть ослаблено (а иногда даже отсутствует) или наоборот усилено. Усиление голосового дрожания наблюдается при уплотнении легочной ткани хорошо проводящей звук (воспаление, инфаркт, туберкулез, ателектаз) или при наличии в легких полости, сообщающейся с бронхами (каверна, абсцесс, бронхоэктазы). Ослабление голосового дрожания может наблюдаться у тучных лиц, при эмфиземе легких, закупорке проводящего бронха, инородным телом, пневмотораксе, гидротораксе, фибротораксе.
 Перкуссия легочных больных Перкуссия легких – это нанесение на грудную клетку перкуторных ударов, приводящих подлежащие органы в колебательные движения, физические характеристики которых (продолжительность звуковых колебаний, их частота, амплитуда и тембровая окраска) зависят от плотности органа, эластичности его структур и содержания в нем воздуха. Способы перкуссии: А) непосредственная перкуссия (по Л. Ауэнбруггеру; по Ф. Г. Яновскому и по В. П. Образцову); Б) посредственную перкуссию с помощью плессиметра и молоточка, перкуссию пальцем по пальцу (П. Пиорри, Г. И. Сокольский); В) пороговую перкуссию по Плешу.
Перкуссия легочных больных Перкуссия легких – это нанесение на грудную клетку перкуторных ударов, приводящих подлежащие органы в колебательные движения, физические характеристики которых (продолжительность звуковых колебаний, их частота, амплитуда и тембровая окраска) зависят от плотности органа, эластичности его структур и содержания в нем воздуха. Способы перкуссии: А) непосредственная перкуссия (по Л. Ауэнбруггеру; по Ф. Г. Яновскому и по В. П. Образцову); Б) посредственную перкуссию с помощью плессиметра и молоточка, перкуссию пальцем по пальцу (П. Пиорри, Г. И. Сокольский); В) пороговую перкуссию по Плешу.


 Основные перкуторные звуки 1. Ясный легочный звук – умеренно продолжительный и относительно низкочастотный, (эталон – подмышечные области здорового человека); 2. Тупой перкуторный звук – малой продолжительности (короткий) и сравнительно высокочастотный, (эталон – над мышцами бедра); 3. Тимпанический звук – продолжительный и относительно низкочастотный, (эталон - над полыми органами); 4. Коробочный – умеренно продолжительный и относительно низкочастотный (главное отличие от ясного легочного звука – отсутствие тембровой окраски, обертонов (пустой), приближается к тимпаническому). Эталоном является звук при перкуссии подушки.
Основные перкуторные звуки 1. Ясный легочный звук – умеренно продолжительный и относительно низкочастотный, (эталон – подмышечные области здорового человека); 2. Тупой перкуторный звук – малой продолжительности (короткий) и сравнительно высокочастотный, (эталон – над мышцами бедра); 3. Тимпанический звук – продолжительный и относительно низкочастотный, (эталон - над полыми органами); 4. Коробочный – умеренно продолжительный и относительно низкочастотный (главное отличие от ясного легочного звука – отсутствие тембровой окраски, обертонов (пустой), приближается к тимпаническому). Эталоном является звук при перкуссии подушки.
 Общие правила перкуссии легких Положение врача и больного должны быть удобным для исследования. Палец – плессиметр плотно прижимается к коже. Палец – молоточек перпендикулярен плессиметру. Правая рука параллельна левой. Наносятся два отрывистых перкуторных удара через короткие временные интервалы. Движения руки осуществляется только в лучезапястном суставе. Руки врача должны быть теплыми.
Общие правила перкуссии легких Положение врача и больного должны быть удобным для исследования. Палец – плессиметр плотно прижимается к коже. Палец – молоточек перпендикулярен плессиметру. Правая рука параллельна левой. Наносятся два отрывистых перкуторных удара через короткие временные интервалы. Движения руки осуществляется только в лучезапястном суставе. Руки врача должны быть теплыми.
 Сравнительная перкуссия легких Проводят сравнение характера перкуторных звуков, полученных на симметричных участках грудной клетки. Наносят удары средней силы или применяют громкую перкуссию. Перкуссия проводится по межреберьям. Последовательность: Спереди перкутируют подключичные зоны, ключицу, первое, второе и третье межреберье справа и слева, палец-плессиметр расположен горизонтально, четвертое и пятое межреберье – справа. Боковые поверхности перкутируют сверху вниз, начиная от границы волосистой части подмышечной области, при этом кожную складку сдвигают вверх. Палец-плессиметр располагается горизонтально в каждом межреберье. Сзади перкутируют надлопаточную область. Палец-плессиметр параллелен и выше ости лопатки. Затем межлопаточную область, палец плессиметр расположен вертикально (для удобства руки больного скрещивают на груди). Подлопаточные области перкутируют ниже углов лопаток. Палец плессиметр расположен горизонтально.
Сравнительная перкуссия легких Проводят сравнение характера перкуторных звуков, полученных на симметричных участках грудной клетки. Наносят удары средней силы или применяют громкую перкуссию. Перкуссия проводится по межреберьям. Последовательность: Спереди перкутируют подключичные зоны, ключицу, первое, второе и третье межреберье справа и слева, палец-плессиметр расположен горизонтально, четвертое и пятое межреберье – справа. Боковые поверхности перкутируют сверху вниз, начиная от границы волосистой части подмышечной области, при этом кожную складку сдвигают вверх. Палец-плессиметр располагается горизонтально в каждом межреберье. Сзади перкутируют надлопаточную область. Палец-плессиметр параллелен и выше ости лопатки. Затем межлопаточную область, палец плессиметр расположен вертикально (для удобства руки больного скрещивают на груди). Подлопаточные области перкутируют ниже углов лопаток. Палец плессиметр расположен горизонтально.
 Над здоровыми легкими определяется ясный легочный звук. При сравнительной перкуссии здорового человека перкуторный звук и в симметричный участках может быть не совсем одинаковым. Более тихий и короткий звук определяется: Над правой верхушкой – за счет более короткого правого верхнего бронха, что уменьшает его воздушность, большего развития мышц правого плечевого пояса; Во 2 -м и 3 -м межреберьях слева, за счет более близкого расположения сердца; Над верхними долями легких, по сравнению с нижними долями, в результате различной толщины воздухосодержащей легочной ткани; В правой подмышечной области, по сравнению с левой, вследствие близости расположения печени, а также вследствие того, что слева к диафрагме и легкому примыкает желудок, дно которого заполнено воздухом и при перкуссии дает громкий тимпанический звук (полулунное пространство Траубе).
Над здоровыми легкими определяется ясный легочный звук. При сравнительной перкуссии здорового человека перкуторный звук и в симметричный участках может быть не совсем одинаковым. Более тихий и короткий звук определяется: Над правой верхушкой – за счет более короткого правого верхнего бронха, что уменьшает его воздушность, большего развития мышц правого плечевого пояса; Во 2 -м и 3 -м межреберьях слева, за счет более близкого расположения сердца; Над верхними долями легких, по сравнению с нижними долями, в результате различной толщины воздухосодержащей легочной ткани; В правой подмышечной области, по сравнению с левой, вследствие близости расположения печени, а также вследствие того, что слева к диафрагме и легкому примыкает желудок, дно которого заполнено воздухом и при перкуссии дает громкий тимпанический звук (полулунное пространство Траубе).
 Притупление или тупой перкуторный звук над легкими свидетельствует о наличии: уплотнения легочной ткани (долевая или очаговая пневмония, обтурационный ателектаз); жидкости в плевральной полости (эксудативный плеврит, гидроторакс, гемоторакс); облитерации полости плевры (фиброторакс). Иногда в начальных стадиях долевого уплотнения легких или над компрессионным ателектазом можно определить притупление перкуторного звука с тимпаническим оттенком. Тимпанический перкуторный звук над легкими выявляется: при пневмотораксе; при наличии большой полости. Коробочный звук выявляется при эмфиземе легких.
Притупление или тупой перкуторный звук над легкими свидетельствует о наличии: уплотнения легочной ткани (долевая или очаговая пневмония, обтурационный ателектаз); жидкости в плевральной полости (эксудативный плеврит, гидроторакс, гемоторакс); облитерации полости плевры (фиброторакс). Иногда в начальных стадиях долевого уплотнения легких или над компрессионным ателектазом можно определить притупление перкуторного звука с тимпаническим оттенком. Тимпанический перкуторный звук над легкими выявляется: при пневмотораксе; при наличии большой полости. Коробочный звук выявляется при эмфиземе легких.
 Топографическая перкуссия легких Определяется верхняя и нижняя границы легких, а также подвижность нижнего края легких. Правила проведения топографической перкуссии легких Проводится точно по топографическим линиям. Сила перкуторного звука – тихая. Перкуссию проводят по ребрам и межреберьям. Направление перкуссии – от легочного к тупому звуку. Палец плессиметр перемещают параллельно границе ожидаемой тупости. Границы легкого отмечают по краю пальца, обращенного к легочному звуку.
Топографическая перкуссия легких Определяется верхняя и нижняя границы легких, а также подвижность нижнего края легких. Правила проведения топографической перкуссии легких Проводится точно по топографическим линиям. Сила перкуторного звука – тихая. Перкуссию проводят по ребрам и межреберьям. Направление перкуссии – от легочного к тупому звуку. Палец плессиметр перемещают параллельно границе ожидаемой тупости. Границы легкого отмечают по краю пальца, обращенного к легочному звуку.
 Определение высоты стояния верхушек (верхних границ) легкого Спереди перкуссию проводят от середины ключицы вверх и медиально по направлению к сосцевидному отростку. В норме расстояние от верхнего края ключицы до найденной границы составляет 3 -4 см. Сзади перкуссию проводят от ости лопатки по направлению к остистому отростку седьмого шейного позвонка на 3 -4 см. в сторону от него. В норме верхушка легких сзади находится на уровне остистого отростка седьмого шейного позвонка. Определение ширины полей Кренига. Палец плессиметр располагаю по верхнему краю трапециевидной мышцы, на ее средине. Перкутируют в медиальном и латеральном направлениях. В норме расстояние между найденными границами равно 5 -8 см.
Определение высоты стояния верхушек (верхних границ) легкого Спереди перкуссию проводят от середины ключицы вверх и медиально по направлению к сосцевидному отростку. В норме расстояние от верхнего края ключицы до найденной границы составляет 3 -4 см. Сзади перкуссию проводят от ости лопатки по направлению к остистому отростку седьмого шейного позвонка на 3 -4 см. в сторону от него. В норме верхушка легких сзади находится на уровне остистого отростка седьмого шейного позвонка. Определение ширины полей Кренига. Палец плессиметр располагаю по верхнему краю трапециевидной мышцы, на ее средине. Перкутируют в медиальном и латеральном направлениях. В норме расстояние между найденными границами равно 5 -8 см.
 Определение нижних границ легких проводят по топографическим линиям справа и слева. Слева по парастернальной и средино - ключичной линиям не определяют из-за имеющийся здесь сердечной тупости. Расположение нижних границ легких в норме Топографические линии Правое легкое Левое легкое Окологрудниная VI межреберье - Средино-ключичная VI ребро - Передняя подмышечная VII ребро Средняя подмышечная VIII ребро Задняя подмышечная IX ребро Лопаточная X ребро Около позвоночная XI ребро
Определение нижних границ легких проводят по топографическим линиям справа и слева. Слева по парастернальной и средино - ключичной линиям не определяют из-за имеющийся здесь сердечной тупости. Расположение нижних границ легких в норме Топографические линии Правое легкое Левое легкое Окологрудниная VI межреберье - Средино-ключичная VI ребро - Передняя подмышечная VII ребро Средняя подмышечная VIII ребро Задняя подмышечная IX ребро Лопаточная X ребро Около позвоночная XI ребро
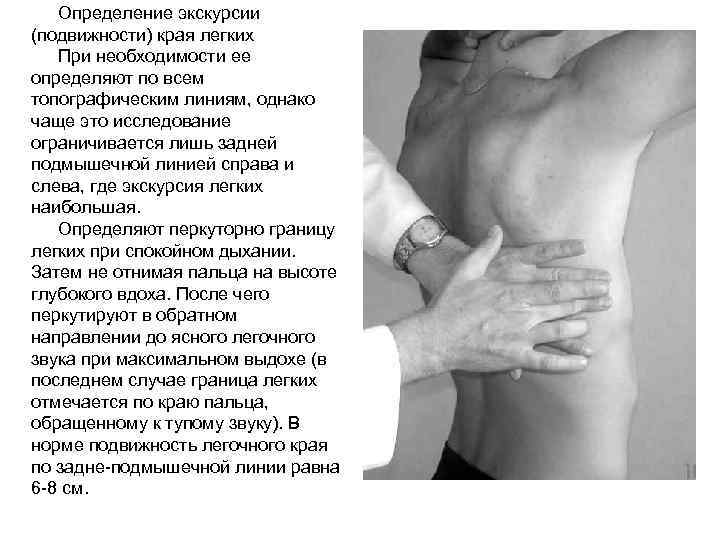 Определение экскурсии (подвижности) края легких При необходимости ее определяют по всем топографическим линиям, однако чаще это исследование ограничивается лишь задней подмышечной линией справа и слева, где экскурсия легких наибольшая. Определяют перкуторно границу легких при спокойном дыхании. Затем не отнимая пальца на высоте глубокого вдоха. После чего перкутируют в обратном направлении до ясного легочного звука при максимальном выдохе (в последнем случае граница легких отмечается по краю пальца, обращенному к тупому звуку). В норме подвижность легочного края по задне-подмышечной линии равна 6 -8 см.
Определение экскурсии (подвижности) края легких При необходимости ее определяют по всем топографическим линиям, однако чаще это исследование ограничивается лишь задней подмышечной линией справа и слева, где экскурсия легких наибольшая. Определяют перкуторно границу легких при спокойном дыхании. Затем не отнимая пальца на высоте глубокого вдоха. После чего перкутируют в обратном направлении до ясного легочного звука при максимальном выдохе (в последнем случае граница легких отмечается по краю пальца, обращенному к тупому звуку). В норме подвижность легочного края по задне-подмышечной линии равна 6 -8 см.
 Пространство Траубе Зона тимпанического перкуторного звука в левом подреберье. Границы: правая – левая граница печени; левая – граница селезенки; верхняя – граница левого легкого; нижняя – край левой реберной дуги
Пространство Траубе Зона тимпанического перкуторного звука в левом подреберье. Границы: правая – левая граница печени; левая – граница селезенки; верхняя – граница левого легкого; нижняя – край левой реберной дуги
 Интерпретация топографической перкуссии 1. Опущение нижних границ легких может встречаться при низком стоянии диафрагмы и эмфиземе легких. 2. Нижние границы легких могут быть приподняты при высоком стоянии диафрагмы, сморщивании (рубцевании) легкого в нижних долях. 3. Опущение верхних границ легких встречается при сморщивании легких, а их поднятие и расширение полей Кренинга – при эмфиземе легких. 4. Следует отметить, что топографическая перкуссия легких имеет важную диагностическую значимость в процессе динамического наблюдения за больным.
Интерпретация топографической перкуссии 1. Опущение нижних границ легких может встречаться при низком стоянии диафрагмы и эмфиземе легких. 2. Нижние границы легких могут быть приподняты при высоком стоянии диафрагмы, сморщивании (рубцевании) легкого в нижних долях. 3. Опущение верхних границ легких встречается при сморщивании легких, а их поднятие и расширение полей Кренинга – при эмфиземе легких. 4. Следует отметить, что топографическая перкуссия легких имеет важную диагностическую значимость в процессе динамического наблюдения за больным.
В пособии приводятся методы исследования и семиологии при заболевании отдельных органов и систем, а также описание основных заболеваний и их лечения. Для студентов высших медицинских учебных заведений, врачей общей практики.
- ЛЕКЦИЯ 1. Болезни органов дыхания. Клинические синдромы при заболевании органов дыхания. Часть 1
- ЛЕКЦИЯ 2. Клинические синдромы при заболевании органов дыхания. Часть 2
- ЛЕКЦИЯ 5. Пневмония. Этиология, патогенез, классификация
- ЛЕКЦИЯ 6. Пневмония. Клинические проявления и диагностика
- ЛЕКЦИЯ 13. Бронхиальная астма. Патогенез и классификация
* * *
Приведённый ознакомительный фрагмент книги Факультетская терапия. Конспект лекций (А. В. Писклов, 2005) предоставлен нашим книжным партнёром - компанией ЛитРес .
ЛЕКЦИЯ 1. Болезни органов дыхания. Клинические синдромы при заболевании органов дыхания. Часть 1
1. Синдром жидкости в плевральной полости
2. Синдром плевральных шумов
3. Синдром воздуха в области плевры
4. Синдром воспалительного уплотнения легочной ткани
Диагностика болезней органов дыхания базируется на клинических, инструментальных, лабораторных критериях. Совокупность отклонений, получаемых при применении различных методов исследования при каком-либо патологическом состоянии, принято называть синдромом.
1. Синдром жидкости в плевральной полости. Характерная жалоба при этом – одышка. Она отражает степень дыхательной недостаточности из-за сдавления легкого плевральным, которая приводит к уменьшению дыхательной поверхности в легких в целом. При осмотре обращают внимание на выпячивание и отставание в акте дыхания соответствующей половины грудной клетки. Голосовое дрожание и бронхотония ослаблены или отсутствуют. При перкуссии определяются укорочение или притупление звука или тупой звук. Аускультативно дыхание ослаблено или отсутствует.
2. Синдром плевральных шумов. Воспаление листков плевры может оставить после себя выраженный внутриплевральный спаечный субстрат в виде спаечных тяжей, сращений, фибринозных плевральных наложений. Жалобы у таких больных могут отсутствовать, но при выраженных спайках появляются одышка и боли в грудной клетке при физической нагрузке. При осмотре грудной клетки отмечаются западение и отставание в акте дыхания пораженной половины: здесь же можно обнаружить втяжение межреберных промежутков на вдохе. Голосовое дрожание и бронхофония ослаблены или отсутствуют. Перкуторный звук притупленный. При аускультации дыхание ослаблено или отсутствует. Часто выслушивается шум трения плевры.
3. Синдром воздуха в полости плевры. Воздух в полости плевры может оказаться при прорыве в нее субплеврально расположенных каверны или абсцесса. Сообщение бронха с плевральной полостью приводит к накоплению в последней воздуха, которое сдавливает легкое. В этой ситуации повышенное давление в плевральной полости может привести к закрытию отверстия в плевре кусочками поврежденной ткани, прекращению поступления воздуха в плевральную полость и формированию закрытого пневмоторакса. Если сообщение бронха с полостью плевры не ликвидируется, пневмоторакс носит название открытого.
В обоих случаях основными жалобами являются резко развивающееся удушье и боли в грудной клетке. При осмотре определяются выпячивание пораженной половины грудной клетки, ослабление участия ее в акте дыхания. Голосовое дрожание и бронхофония при закрытом пневмотораксе – ослабленные или отсутствуют, при открытом – усиленные. При перкуссии в обоих случаях определяется тимпанит. Аускультативно при закрытом пневмотораксе дыхание резко ослаблено или отсутствует, при открытом – дыхание бронхиальное. В последнем случае может выслушиваться металлическое дыхание как разновидность бронхиального дыхания.
4. Синдром воспалительного уплотнения легочной ткани. Уплотнение легочной ткани может возникнуть не только в результате воспалительного процесса (пневмония), когда альвеолы заполняются экссудатом и фибрином. Уплотнение может произойти в результате инфаркта легкого, когда альвеолы заполняются кровью, при отеке легких, когда в альвеолах скапливается отечная жидкость – транссудат. Однако уплотнение легочной ткани воспалительного характера встречается наиболее часто. При поражении целой доли легкого развивается долевая либо крупозная пневмония; одного или нескольких сегментов – полисегментарная пневмония; менее одного сегмента – очаговая пневмония.
Больные предъявляют жалобы на кашель, одышку, при вовлечении в воспалительный процесс плевры – на боли в грудной клетке. При осмотре – пораженная половина грудной клетки отстает в акте дыхания, что характерно для лобарной пневмонии. Голосовое дрожание и бронхофония в зоне уплотнения усилены. Перкуторный звук при очаговой пневмонии притупленный (не тупой), так как участок уплотненной легочной ткани окружен нормальной тканью легкого. При долевой пневмонии в начальной стадии звук притупленно-тимпанический, в стадии разгара – тупой, который в стадии разрешения постепенно сменяется ясным легочным звуком.
При очаговой пневмонии аускультативно выявляется смешанное (бронховезикулярное) дыхание. Слышны сухие и влажные хрипы, при этом влажные хрипы характеризуются как звучные, поскольку воспалительное уплотнение легочной ткани вокруг бронхов способствует лучшему проведению на поверхность грудной клетки зарождающихся в них влажных хрипов. При глубоком расположении очага воспаления каких-либо отклонений при физикальном исследовании выявить не удается. В то же время очаг воспаления большой величины, находящийся в непосредственной близости от висцеральной плевры, дает при физикальном исследовании такие же отклонения, как и крупозная пневмония.
При крупозной пневмонии аускультативно на стороне поражения в начальной стадии выявляется ослабление везикулярного дыхания, крепитация и шум трения плевры, в стадии разгара выслушивается бронхиальное дыхание, может быть шум трения плевры. В стадии разрешения бронхиальное дыхание постепенно сменяется везикулярным, появляется крепитация, влажные звучные хрипы из-за проникновения разжиженного экссудата их альвеол, возможен шум трения плевры.
3. Синдром инфильтративного (или очагового) уплотнения легочной ткани
Это патологическое состояние, обусловленное проникновением в ткани легкого и накоплением в них клеточных элементов, жидкостей, различных химических веществ. Оно складывается из характерных морфологических, рентгенологических и клинических проявлений.
Инфильтрация может быть лейкоцитарной, лимфоцитарной, макрофагальной, эозинофильной, геморрагической. Лейкоцитарные инфильтраты часто осложняются нагноительными процессами (абсцесс легкого). Клиника зависит от заболевания, вызвавшего инфильтрат (например, пневмония, туберкулез). Имеет значение площадь поражения.
В клинике синдрома преобладают:
- - Кашель.
- - Одышка.
- - Кровохарканье.
- - Боли в грудной клетке (при субплевральном расположении очага).
- - Общие симптомы (температура, потливость, слабость и др.).
При аускультации наблюдается ослабленное везикулярное дыхание, притупление перкуторного звука, на противоположной стороне может быть усиленное везикулярное дыхание. Из патологических дыхательных шумов могут выслушиваться сухие и влажные хрипы.
4. Синдром воздушной полости в легких
Воздушная полость возникает в результате деструкции легочной ткани (например, абсцесс, каверна). Может сообщаться или не сообщаться с бронхом.
В симптоматике этого синдрома преобладают:
- - Кашель.
- - Кровохарканье.
- - Боли в грудной клетке на стороне поражения.
- - Большое количество мокроты при больших размерах полости (при бронхоэктазах).
- - Симптомы интоксикации.
При аускультации над полостью выслушивается бронхиальное дыхание и влажные хрипы. Для подтверждения диагноза проводят рентгенологическое, бронхографическое исследования.
5. Синдром ателектаза
Ателектаз -- это патологическое состояние легкого или его части, при котором легочные альвеолы не содержат воздуха, в результате чего их стенки спадаются. Ателектаз может быть врожденным и приобретенным.
- 1. Обтурационный ателектаз -- при полном или почти полном закрытии просвета бронха. При этом возникает
:
- а) пароксизмальная одышка,
- б) упорный сухой кашель,
- в) диффузный цианоз,
- г) тахипноэ,
- д) западение пораженной половины грудной клетки со сближением ребер.
- 2. Компрессионный ателектаз -- при внешнем сдавлении легочной ткани из-за объемных процессов (например, при экссудативном плеврите).
- 3. Дистензионный (или функциональный) ателектаз -- при нарушении условий для расправления легкого на вдохе. Возникает у ослабленных больных после наркоза, при отравлении барбитуратами, из-за угнетения дыхательного центра. Обычно это небольшой участок легочной ткани в нижних отделах легких. Развитие этого ателектаза мало отражается на дыхательной функции.
- 4. Смешанные (парапневмонические) ателектазы - при сочетании обтурации бронхов, компрессии и дистензии легочной ткани.
Все формы ателектаза, за исключением дистензионного, являются грозным осложнением, при котором врач должен быть особо внимателен.
6. Синдром повышенной воздушности легочной ткани (эмфизема)
Эмфизема -- это патологическое состояние, которое характеризуется расширением воздушных пространств легких, расположенных дистальнее герминальных бронхов, наступающее из-за снижения эластичности легочной ткани.
Она может быть первичной и вторичной. В развитии этого синдрома играет роль расстройство кровообращения в сети легочных капилляров и разрушение альвеолярных перегородок. Легкое утрачивает эластичность и силу эластической тяги. В результате стенки бронхиол спадаются. Этому способствуют различные физические и химические факторы (например, эмфизема у музыкантов, играющих на духовых инструментах), заболевания органов дыхания, при которых развивается обструкция мелких бронхов (обструктивный или дистальный бронхит), нарушение функции дыхательного центра в регуляции вдоха и выдоха.
- - Одышка (непостоянная, экспираторная).
- - Кашель.
При перкуссии над легкими -- звук с коробочным оттенком. Дыхание ослабленное («ватное»).
7. Синдром скопления жидкости в плевральной полости
Это клинико-рентгенологический и лабораторный симптомокомплекс, обусловленный жидкостью, скапливающейся в плевральной полости или из-за поражения плевры, или из-за общих электролитных нарушений в организме. Жидкость может быть экссудатом (при воспалении), транссудатом (гемоторакс). Если транссудат состоит из лимфы, то это -- хилоторакс (возникает при повреждении грудного лимфатического протока, при туберкулезе средостения или опухоли средостения). Жидкость поджимает легкое, развивается компрессия альвеол.
- - Одышка.
- - Боли или чувство тяжести в грудной клетке.
- - Общие жалобы.
- 8. Синдром скопления воздуха в плевральной полости (пневмоторакс)
Пневмоторакс -- это патологическое состояние, характеризующееся скоплением воздуха между париетальной и висцеральной плеврой.
Может быть односторонним и двусторонним, частичным и полным, открытым и закрытым.
Причины: повреждение грудной клетки (посттравматический), спонтанный, искусственный (при лечении туберкулеза).
- - Острая дыхательная и правожелудочковая недостаточность (поверхностное дыхание, цианоз).
- - Грубое бронхиальное дыхание, отсутствие везикулярного дыхания (табл. 2).
- 9. Дыхательная недостаточность
Дыхательная недостаточность -- это патологическое состояние организма, при котором либо не обеспечивается поддержание нормального газового состава крови, либо он достигается такой работой дыхательного аппарата, которая снижает функциональные возможности организма.
Основными механизмами развития этого синдрома являются нарушение процессов вентиляции альвеол, диффузии молекулярного кислорода и углекислого газа и перфузии крови через каппилярные сосуды.
Обычно развивается у больных, страдающих хроническими заболеваниями легких, с наличием эмфиземы и пневмосклероза, но может быть у пациентов с острыми болезнями, с выключением из дыхания большой массы легких (пневмония, плеврит).
Существует 3 типа нарушения вентиляции легких:
- - Обструктивный.
- - Рестриктивный.
- - Смешанный.
Дыхательная недостаточность может быть первичной и вторичнойу острой и хронической, латентной и явной, парциальной и глобальной.
Клинически дыхательная недостаточность проявляется одышкой, тахикардией, цианозом и при крайней степени выраженности может сопровождаться нарушением сознания и судорогами.
О степени дыхательной недостаточности судят по функциональным показателям аппарата внешнего дыхания.
Существует клиническая классификация дыхательной недостаточности:
І степень -- одышка возникает только при физическом напряжении;
ІІ степень -- появление одышки при незначительной физической нагрузке;
ІІІ степень -- наличие одышки в покое.
Выделение синдромов является важным этапом диагностического процесса при заболеваниях легких, который завершается определением нозологической формы заболевания.
10. Легочное кровотечение
Синдром диффузного альвеолярного кровотечения представляет собой персистирующее или повторяющееся легочное кровотечение. Чаще такие кровотечения диагностируют при туберкулезе легких (40-66%), нагноительных заболеваниях легких (30-33%), раке лёгкого (10-15%).
Причина: изолированный иммунный легочный капиллярит - микрососудистый васкулит, ограниченный поражением сосудов легких; его единственное проявление - альвеолярное легочное кровотечение, возникающее у людей в возрасте 18-35 лет.
Идиопатический легочный гемосидероз - синдром диффузного альвеолярного кровотечения, при котором невозможно выявить основное заболевание. Легочное кровотечение встречается главным образом у детей младше 10 лет и, как считается, возникает вследствие дефекта в альвеолярном капиллярном эндотелии, возможно, из-за аутоиммунного повреждения.
Некоторые из этих заболеваний могут также вызвать гломерулонефрит, в этом случае говорят, что у пациента имеет место легочно-почечный синдром.
Основные источники легочного кровотечения
- - Аневризмы Расмуссена (аневризма легочной артерии, проходящей через туберкулезную каверну).
- - Варикозно расширенные вены, проходящие через фиброзную, перибронхи- альную и интраальвеолярную цирротическую ткань.
- - Ветви легочной артерии.
- - Бронхиальные артерии.
Анастомозы между легочной артерией и бронхиальными артериями.
- - Тонкостенные сосудистые сплетения (типа гемангиом), формирующиеся в зонах хронического воспаления и пневмосклероза.
- - Воспаленные или окаменевшие бронхопульмональные лимфатические узлы, их наличие обусловливает формирование некроза сосудистой стенки.
- - Диапедезные легочные кровотечения, развившиеся из-за нарушения проницаемости капилляров в результате воспаления сосудистой стенки или воздействия на нее токсинов.
Симптомы и проявления умеренного синдрома диффузного альвеолярного легочного кровотечения - одышка, кашель и лихорадка; однако у многих пациентов развивается острая дыхательная недостаточность. Кровохарканье встречается часто, но у трети пациентов может отсутствовать. Дети с идиопатическим легочным гемосидерозом могут иметь выраженное отставание в развитии. При физикальном обследовании специфические симптомы не обнаруживаются.
Осложнения
Асфиксия - наиболее опасное осложнение легочного кровотечения. Иногда обнаруживают ателектазы. В результате легочного кровотечения происходит прогрессирование основного процесса, это отмечают и при туберкулезе, и при гнойных заболеваниях легких.
Пневмония, традиционно называемая гемоаспирационной, - типичное и часто возникающее осложнение легочного кровотечения МКБ-10 содержит два различных понятия пневмонию (заболевание легких инфекционного характера) и пневмонит (состояние, вызванное гемоаспирацией). Под гемоаспирационной пневмонией следует понимать пневмонит, возникший вследствие аспирации крови, осложненный присоединением инфекционной флоры.
Диагностика легочного кровотечения
В диагностике легочного кровотечения большое значение имеет рентгенография и КТ. Однако наиболее информативным диагностическим методом считают бронхоскопию, позволяющую определить не только сторону кровотечения, но и обнаружить его источник.
Рассмотрим также бронхоспастический синдром и остановимся на синдроме бронхиальной обструкции более подробно. Здесь необходимо ввести понятие бронхитического синдрома.
11. Бронхитический синдром
Бронхитический синдром формируется при поражении трахеобронхиального дерева и включает в себя синдром бронхиальной обструкции и бронхоспастический синдром.
12. Синдром бронхиальной обструкции
Синдром бронхиальной обструкции -- это клинический симптомокомплекс, ведущим признаком которого является экспираторная одышка, возникающая вследствие ограничения воздушного потока в бронхиальном дереве, преимущественно на выдохе, обусловленного бронхоспазмом, отеком слизистой оболочки бронхов и дискринией. Под последним термином понимается повышенная продукция закупоривающего просвет бронхов патологического бронхиального секрета с измененными свойствами (в первую очередь повышенная вязкость), нарушающая мукоцилиарный клиренс. Другое общепринятое название этого патологического состояния -- бронхообструктивный синдром.
Синдром бронхиальной обструкции в подавляющем большинстве случаев является результатом дегенеративно-дистрофических изменений и/или воспалительного процесса в слизистой оболочке бронхиального дерева, чаще -- его дистальных отделов, вследствие разнообразных причин экзо- и эндогенного происхождения. Бронхиальная обструкция может быть проявлением острого заболевания -- острого бронхита и очаговой пневмонии. Однако чаще всего она является основным клиническим синдромом хронического обструктивного заболевания легких и бронхиальной астмы. Нередко проявления бронхиальной обструкции встречаются при бронхоэктатической болезни, муковисцидозе, туберкулезе легких, кистозной гипоплазии легких и целом ряде других заболеваний.
13. Патофизиологические механизмы синдрома бронхиальной обструкции
Развитие бронхиальной обструкции обусловлено сложной морфофункциональной перестройкой стенки бронхиального дерева на всем его протяжении под длительным воздействием табачного дыма, пыли, поллютантов, токсических газов, аллергенов, повторных респираторных инфекций (вирусной и бактериальной -- преимущественно Haemophilus influenzae, Moraxella catarrhalis, Streptococcus pneumoniae), с развитием в ней персистирующего воспаления (основные клетки -- нейтрофилы, эозинофилы, макрофаги, тучные клетки). Повреждающее действие указанных патологических факторов приводит к утолщению (вначале обратимому) стенки бронхов вследствие отека подслизистого слоя и гиперплазии расположенных в нем бронхиальных желез, гипертрофии гладкой мускулатуры, фиброзным изменениям.
Уже на ранних этапах развития патологического процесса определяется усиление секреторной активности бокаловидных клеток, увеличение их количества, что сопровождается повышением продукции слизистого секрета с большой молекулярной массой. Указанные изменения сопровождаются снижением функциональной активности микроворсинок мерцательного эпителия, нарушениями в системе сурфактанта.
Следствием всех вышеуказанных изменений является мукоцилиарная недостаточность, сужение просвета воздухоносных путей и увеличение бронхиального сопротивления. Нужно отметить, что бронхиальная обструкция и мукоцилиарная недостаточность являются звеньями (лучше сказать -- стадиями) одного патологического процесса. В первой стадии преобладает мукоцилиарная недостаточность, а во-второй -- бронхиальная обструкция. Бронхиальной обструкции не может быть без мукоцилиарной недостаточности. Однако последняя может и не сопровождаться явлениями бронхиальной обструкции. Классический клинический пример -- хронический бронхит.
Следует также отметить, что в механизмах развития бронхиальной обструкции играют роль расстройства вегетативной нервной регуляции. В норме в регуляции тонуса бронхов участвует симпатическая и парасимпатическая нервная система. Так, по блуждающему нерву передаются влияния, вызывающие сокращения гладких мышц бронхов, а через легочные симпатические сплетения -- адренергические влияния, расслабляющие эти мышцы. В процессе развития бронхиальной обструкции происходит изменение соотношения симпатической и парасимпатической иннервации в пользу преобладания последней. При этом в легких изменяются соотношения адренорецепторов и холинорецепторов в пользу преобладания числа холинергических структур, возбуждение которых приводит не только к сужению бронхов, но и к стимуляции секреции бронхиальных желез.
Распределение рецепторных структур на различных уровнях бронхиального дерева свидетельствует о том, что адренергические рецепторы распределены относительно равномерно с некоторым преобладанием рецепторов на уровне средних и мелких бронхов. Максимальная же плотность холинергических рецепторов, преимущественно мускариновых, отмечается на уровне крупных и меньше -- средних бронхов. По современным представлениям, различают три подтипа мускариновых рецепторов: M1, М2 и М3 . М1 рецепторы шире представлены в парасимпатических ганглиях, М2 -- на окончаниях постганглионарных холинергических волокон, М3 -- на эффекторных клетках гладкой мускулатуры бронхов или клетках-мишенях (преимущественно на тучных клетках и секреторных клетках бронхиального эпителия).
Главным патофизиологическим критерием бронхиальной обструкции является ограничение скорости воздушного потока, особенно экспираторного. При этом наблюдаются значительные нарушения механики дыхания, вентиляционно-перфузионных соотношений и регуляции вентиляции. Результатом является ухудшение альвеолярной вентиляции и снижение оксигенации крови. Недостаточное время выдоха и повышенное бронхиальное сопротивление приводят к увеличению конечно-экспираторного объема легких, уплощению (укорочению) диафрагмы, что ставит её механическую деятельность в невыгодное положение. Активное использование при этом других дополнительных мышц выдоха ещё больше увеличивает потребность организма в кислороде. При отсутствии адекватного лечения у пациента со значительным ограничением воздушного потока может быстро наступить утомление дыхательных мышц, приводящее к снижению эффективности работы дыхания, усугублению артериальной гипоксемии и возникновению гиперкапнии.
Указанные патологические процессы могут усугубляться коллапсом мелких бронхов при потере легкими эластических свойств, развитием обструктивной эмфиземы, облитерацией терминальных бронхиол, трахеобронхиальной дискинезией.
14. Клиническая картина бронхообструктивного синдрома
Синдром бронхиальной обструкции проявляется следующими симптомами:
- - экспираторной одышкой, которая усиливается при физической нагрузке и часто ночью. В тех случаях, когда одышка внезапно возникает на фоне предшествующего нормального дыхания, сопровождается мучительным ощущением удушья и продолжается несколько часов, говорят о приступе удушья;
- - кашлем с отхождением вязкой слизистой или слизисто-гнойной мокроты. После отхождения мокроты состояние больного часто улучшается;
- - ослабленным голосовым дрожанием, коробочным перкуторным звуком, ослабленным везикулярным дыханием с удлиненным выдохом -- симметрично над легкими с обеих сторон;
- - сухими свистящими хрипами над легкими с обеих сторон, которые часто слышны и дистанционно;
- -участием в акте дыхания вспомогательной дыхательной мускулатуры, особенно при выдохе;
- - при тяжелом состоянии -- вынужденным положением тела пациента сидя с фиксацией плечевого пояса, цианозом его видимых слизистых оболочек, иногда -- акроцианозом.
У пациентов с длительным "стажем" бронхиальной обструкции нередко определяется дефицит массы тела, эмфизематозный тип грудной клетки. .Перкуторные и аускультативные данные у таких больных во многом зависят от степени бронхиальной обструкции и выраженности эмфиземы легких.
15. Диагностика и дифференциальная диагностика синдрома бронхиальной обструкции
Обычно клинические проявления бронхиальной обструкции не вызывают сомнения в диагнозе. Однако требует повышенного внимания дифференциальная диагностика бронхиальной обструкции со стенозом (обструкцией) верхних дыхательных путей (чаще гортани) и трахеи. Последняя патология наиболее часто встречается при истинном (дифтерийном) и ложном крупе, опухолях гортани и трахеи, рубцовом стенозе трахеи, чаще всего возникающем после проведения ИВЛ с длительной интубацией трахеи. Дифтерийный и ложный круп встречаются преимущественно у детей в связи с анатомическими особенностями детской гортани.
В клинической картине заболеваний с поражением гортани и трахеи преобладает одышка, в основном смешанная. Во многих случаях клинически трудно определить характер одышки. Кашель беспокоит редко, чаше сухой, "лающий". Предшествовать заболеванию могут изменения голоса, его осиплость. Клиническим исследованием над легкими выявляется так называемое стридорозное дыхание -- громкое бронхиальное дыхание, которое "накладывается" на везикулярное дыхание. Выслушиваются также сухие свистящие хрипы в обе фазы дыхания. Правильному диагнозу в этих сложных случаях помогают тщательно собранный анамнез (изменения голоса, его осиплость, длительная интубация трахеи и искусственная вентиляция легких, трахеотомия в недалеком прошлом, пр.), проведение спирографии с регистрацией и анализом кривой "поток--объем" форсированного дыхания, а также фибробронхоскопии.
В клинической практике большое значение имеет также дифференциация синдрома бронхиальной обструкции при двух основных заболеваниях -- бронхиальной астме и хроническом обструктивном заболевании легких.
При бронхиальной астме бронхиальная обструкция лабильная на протяжении суток, ее симптомы быстро возникают, продолжаются несколько часов и так же быстро самопроизвольно или под действием лечения проходят. Клинически это проявляется приступами удушья -- тяжёлой приступообразной экспираторной одышкой. В период между приступами больные чувствуют себя удовлетворительно и жалоб со стороны органов дыхания, как правило, не предъявляют. Поэтому основными признаками бронхиальной астмы считаются вариабельная и обратимая бронхиальная обструкция в сочетании с гиперреактивностью бронхов -- повышенной их чувствительностью к различным раздражающим факторам (аллергенам, холоду, физической нагрузке, сильным эмоциям, медикаментам, запахам химических веществ).
При хроническом обструктивном заболевании легких (XОЗЛ) бронхиальная обструкция более стойкая на протяжении суток, менее подвержена изменениям при воздействии холода, физической нагрузки и других раздражающих факторов. При каждом обострении воспалительного процесса в трахеобронхиальном дереве она постепенно возрастает из года в год. Такая бронхиальная обструкция более рефрактерна (устойчивая) к проводимой бронходилатационной терапии. Течение заболевания чаше проявляется эмфиземой легких и легочно-сердечной недостаточностью.
Дифференциальной диагностике существенно помогают лабораторные и функциональные методы исследования. В анализе мокроты при бронхиальной астме аллергического происхождения часто встречаются кристаллы Шарко-Лейдена и спирали Куршмана. Среди лейкоцитов преобладают эози- нофилы, а не нейтрофилы и макрофаги, присутствие которых в мокроте более характерно для ХОЗЛ.
Из функциональных методов исследования для дифференциальной диагностики обструкции дыхательных путей наиболее часто применяют спирографию с регистрацией кривой "поток-объем" форсированного дыхания. Свидетельством обструктивного типа легочной недостаточности является снижение объемной скорости воздушного потока. При этом, как правило, определяется снижение < 80% от должных величин ФЖЕЛ, ОФВ1 а также индекса Тиффно -- соотношения OOB1/ФЖЕЛ в %.
В зависимости от преимущественного места ограничения дыхательного потока различают обструкцию верхних дыхательных путей и трахеи, а также нарушения бронхиальной проходимости (бронхиальную обструкцию).
Обструкция верхних дыхательных путей и трахеи на основе анализа петли "поток--объем" делится на три основных функциональных типа: фиксированная обструкция (стеноз трахеи), переменная внутригрудная обструкция (опухоли трахеи) и переменная внегрудная обструкция (опухоли голосовых связок, паралич голосовой связки).
При фиксированной обструкции, геометрия которой остается неизменной (постоянной) в обеих фазах дыхания, ограничивается воздушный поток как на вдохе, так и на выдохе. При этом контур экспираторного потока совпадает с инспираторным. Экспираторная кривая становится плоской и лишена верхушки.
Переменная внегрудная обструкция вызывает избирательное ограничение объемной скорости потока воздуха во время вдоха (ослабление инспираторного потока). Форсированный выдох увеличивает внутритрахеальное давление (Ptr), которое становится выше атмосферного (Patm) Во время вдоха Ptr становится меньше Рatm обусловливая спадание стенок дыхательных путей и соответствующее снижение инспираторного потока.
При переменной внутригрудной обструкции компрессия воздухоносных путей избирательно усиливается во время выдоха. Форсированный выдох увеличивает внутриплевральное давление (Ppl), которое превышает Ptr, вызывая компрессию внутригрудного участка трахеи. Развивается обструкция дыхательных путей на выдохе. Вследствие этого экспираторный поток снижается, а его кривая уплощается. Во время вдоха объемная скорость потока и форма петли остаются в норме.
Нарушения бронхиальной проходимости (бронхиальная обструкция) проявляются так называемым провисанием кривой "поток--объем" форсированного выдоха сразу после достижения пика потока в сочетании с другими признаками обструктивного типа дыхательной недостаточности (снижение ОФВ1).
В зависимости от конфигурации кривой в этой области можно выделить два варианта бронхиальной обструкции: обструкция центральных (больших) бронхов и обструкция периферических (мелких) бронхов. Для первого варианта бронхиальной обструкции характерно резкое снижение объемной скорости форсированного выдоха в начале спадающей ветви кривой "поток--объем". При этом максимальная объемная скорость на уровне выдоха 75% ФЖЕЛ (МОС75, или FEF25), оставшейся в легких, снижается сильнее, чем максимальная объемная скорость на уровне выдоха 50% ФЖЕЛ (МОС50, или FEF50) и максимальная объемная скорость на уровне выдоха 25% ФЖЕЛ (МОС25, или FEF75), оставшихся в легких. Обструкция мелких бронхов, наоборот, характеризуется преимущественным снижением МОС25 (или FEF75) и МОС50 (или FEF50), а также сдвигом экспираторной кривой влево.
Для оценки обратимости бронхиальной обструкции чаще всего применяется фармакологический бронходилатационный тест с в2-агонистами (адреностимуляторами) короткого действия. Из последних препаратов в Украине применяются сальбутамол и фенотерол. Перед проведением теста пациенту необходимо в течение минимум 6 ч воздерживаться от применения бронхолитиков короткого действия. Сначала записывается исходная кривая "поток-объем" форсированного дыхания. Затем пациент вдыхает 1--2 разовые дозы в2-агониста короткого действия. Через 15--30 мин снова записывается кривая "поток--объем" форсированного дыхания. Обструкция считается обратимой или бронходилататор-реактивной, если показатель ОФВ1 улучшается на 15% и более от исходного. Обратимая бронхиальная обструкция более характерна для бронхиальной астмы, а не для ХОЗЛ.
В алгоритме дифференциальной диагностики обструктивных поражений верхних и нижних дыхательных путей экспираторная или недифференцируемая одышка служит основанием для назначения спирографии с регистрацией кривой "поток-объем" форсированного дыхания. Результаты и тщательный анализ этого исследования, при необходимости включающего бронходилатационный тест, дают возможность проведения топической диагностики уровня и обратимости обструктивных нарушений. На определенных этапах диагностического поиска необходимо проведение фибробронхоскопии, которая в большинстве случаев дает возможность уточнить характер и причину выявленных изменений.
16. Лечение синдрома бронхиальной обструкции
Ведущим принципом лечения синдрома бронхиальной обструкции является воздействие на основные патогенетические звенья патологического процесса -- бронхоспазм, воспаление и отек слизистой оболочки бронхов, дискринию. Определяющим объем и особенности фармакотерапии является вид бронхиальной обструкции -- обратимой и вариабельной, клинически проявляющейся приступами удушья, или только частично обратимой/необратимой обструкцией, вызывающей постоянную одышку, усиливающуюся при физических нагрузках.
Основными препаратами, воздействующими на бронхоспазм, являются современные ингаляционные антихолинергические средства, в2-агонисты короткого и пролонгированного действия, метилксантины.
К антихолинергическим средствам, или холинолитикам, которые воздействуют на ацетилхолиновые рецепторы бронхов, принадлежат ипратропиум бромид и тиотропиум бромид. Механизм их действия реализуется за счет уменьшения рефлекторной бронхиальной обструкции на уровне мускариновых рецепторов блуждающего нерва. Эти препараты являются конкурентными антагонистами ацетилхолина. Ипратропиум бромид связывается с М2- и М3-мускариновыми рецепторами, а тиотропиум бромид -- с M1- и М3-мускариновыми рецепторами бронхов. В настоящее время считают, что парасимпатический тонус бронхов является основным обратимым компонентом бронхиальной обструкции при хроническом обструктивном заболевании легких. Снижение парасимпатического тонуса бронхов является также патогенетически оправданным и клинически эффективным у лиц с ночными симптомами бронхиальной астмы. Указанные ингаляционные холинолити- ки, благодаря низкой всасываемости из слизистой оболочки бронхов, не обусловливают системных побочных действий. При их длительном применении снижается повышенный тонус бронхов благодаря релаксации гладкой мускулатуры, блокируется рефлекторный бронхоспазм, уменьшается гиперсекреция слизи бронхиальными железами и бокаловидными клетками. Следствием указанных эффектов является уменьшение кашля и одышки, ночных симптомов заболевания, а также количества отделяемой мокроты. Препараты широко применяются при сопутствующих заболеваниях сердечно-сосудистой системы, так как не вызывают тахикардии и других нарушений сердечного ритма.
Хорошо известно, что стимуляция в2-адренорецепторов, расположенных в большом количестве на уровне мелких бронхов, обусловливает выраженный бронходилатационный эффект. Современные в2-агонисты имеют избирательное действие на в2-адренорецепторы и обычно не блокируют их при длительном применении. Взаимодействие их с рецепторами активирует аденилатциклазу, обусловливая увеличение внутриклеточной концентрации цАМФ и стимуляцию работы кальциевого насоса. Результатом этого является уменьшение концентрации ионов кальция в миофибриллах и дилатация бронхов.
Из в2-агонистов короткого действия чаще всего применяют два препарата -- сальбутамол и фенотерол. Их выпускают в форме аэрозольныхдозирующих ингаляторов или сухопорошковых ингаляторов, использующих для доставки разовой ингаляционной дозы лекарства силу вдоха пациента. Назначают эти препараты в дозе 1--2 ингаляции одноразово для купирования острых симптомов бронхоспазма или в составе базисной бронходилатационной терапии. Их действие начинается через несколько минут после ингаляции и продолжается около 4--6 ч. Частота применения -- не более 4--6 раз в сутки. Сальбутамол отличается большей безопасностью применения. Препарат не подвергается метилированию и не превращается в метаболиты с блокирующей рецепторы активностью. Фенотерол является полным в2-агонистом. Поэтому значительное превышение суточной и разовой дозы этого препарата, которое не контролируется врачом, приводит к формированию порочного круга, когда рецидивирующие симптомы заболевания вынуждают пациента к более частому употреблению все увеличивающихся доз препарата. При этом действие препарата искажается и приводит к развитию так называемого синдрома рикошета. Суть последнего заключается в том, что продукты распада препарата блокируют в2-адренорецепторы бронхов и употребление лекарства становится неэффективным. Частое бессистемное применение больших доз (20--30 ингаляционных доз в сутки и более) в2-адреномиметиков (чаше фенотерола и формотерола) может привести к тахифилаксии, токсическому действию на сердце, возникновению опасных аритмий и даже "летальному концу с ингалятором в руке", описанному в литературе.
Широкое применение при лечении синдрома бронхиальной обструкции приобрели комбинированные препараты, в которых используется сочетаниев2-агонистов короткого действия с холинолитиками. К ним принадлежат ипратропиум бромид/фенотерол и ипратропиум бромид/сальбутамол, которые выпускаются в форме аэрозольных дозирующих ингаляторов. Эти препараты назначают по 1--2 ингаляционные дозы 3--4 раза в сутки. Максимальный бронхолитический эффект достигается через 30--60 мин после ингаляции, поэтому их можно применять не только в составе базисной бронходилатационной терапии, но также для купирования острых симптомов бронхоспазма.
Для проведения базисной бронходилатационной терапии более целесообразным является применение в2-агонистов пролонгированного действия -- салметерола и формотерола, продолжительность действия которых превышает 12 ч. Длительное плановое применение этих препаратов позволяет эффективно контролировать симптомы бронхиальной обструкции, уменьшить частоту обострений и существенно улучшить качество жизни пациентов. Кроме того, в2-агонисты пролонгированного действия обладают целым рядом других свойств, положительно влияющих на течение патологического процесса. Они снижают степень нейтрофильного воспаления, уменьшая отек слизистой оболочки бронхов, снижают проницаемость капилляров, уменьшают высвобождение медиаторов воспаления, улучшают мукоцилиарный клиренс. Салметерол назначают чаще всего по 2 разовые дозы 1--2 раза в сутки. Он хорошо сочетается с холинолитиками и метилксантинами, а также с ингаляционными ГКС.
В случае превалирования у больного ночной симптоматики и/или малой эффективности холинолитиков и Рг-агонистов в лечебные схемы следует ввести метилксантины -- препараты теофиллина. Механизм их действия заключается в угнетении активности фосфодиэстеразы, что обусловливает повышение внутриклеточной концентрации цАМФ. В настоящее время установлено, что повышение концентрации цАМФ может быть также результатом стимуляции этими препаратами пуриновых рецепторов. Несмотря на более слабый бронхолитический эффект, теофиллины имеют некоторые преимущества:
улучшают мукоцилиарный клиренс -- работу реснитчатого эпителия;
улучшают сократительную способность дыхательных мышц и уменьшают их усталость;
стимулируют дыхательный центр и работу надпочечников;
обладают мочегонным эффектом и слабым противовоспалительным действием;
потенцируют эффект в2-агонистов короткого действия и холинолитиков.
Однако эти препараты имеют узкий терапевтический диапазон и многочисленные побочные эффекты. Поэтому при их применении необходим мониторинг сывороточной концентрации. Оптимальным считается содержание 10-20 мг препарата в 1 л крови. Теофиллины назначают внутрь, внутривенно и ректально в виде свечей. Для базисной бронходилатационной терапии чаще всего применяют пероральное введение теофиллинов пролонгированного действия 2 раза в сутки. В случае острого бронхоспазма вводят внутривенно аминофиллин.
Основными противовоспалительными средствами, применяющимися для лечения синдрома бронхиальной обструкции, являются кромоны, модификаторы лейкотриенов и глюкокортикостероидные гормоны.
Кромоны одновременно служат средствами профилактической и базисной противовоспалительной терапии. Основу их фармакологического действия составляет стабилизация мембран тучных клеток и базофилов, предупреждающая процесс дегрануляции, а также угнетение активности фосфодиэстеразы с повышением внутриклеточной концентрации цАМФ. Применение кромонов является эффективным при обратимой и вариабельной бронхиальной обструкции, преимущественно аллергического происхождения. Их можно использовать для профилактики развития приступа удушья перед ожидаемым контактом с аллергеном или перед физической нагрузкой. В настоящее время в эту группу входят два препарата -- кромогликат натрия и недокромил натрия.
Кромогликат натрия выпускается в двух медикаментозных формах: в виде порошка в капсулах, содержащих разовую дозу, вместе с доставочным устройством -- спинхалером, а также в виде аэрозольного дозирующего ингалятора. В целях профилактики назначают 1-2 ингаляции разовой дозы препарата, а при продолжающемся контакте с аллергеном препарат ингалируется в аналогичной дозе 4 раза в день до прекращения контакта с аллергеном. Препарат можно применять в составе базисной противовоспалительной терапии по 2 разовые дозы 3-4 раза в сутки на протяжении нескольких месяцев.
Недокромил натрия является лекарством, которое по силе противовоспалительного эффекта в несколько раз превышает действие кромогликата натрия. Особенно эффективно применение недокромила натрия у детей и лиц молодого возраста с проявлениями атопии для лечения поллиноза с астматическим синдромом. Медикаментозной формой препарата является аэрозольный дозирующий ингалятор. Биодоступность лекарства низкая, побочные эффекты наблюдаются очень редко. С профилактической целью назначают 2 ингаляции разовой дозы. При продолжающемся контакте с аллергеном препарат ингалируется в аналогичной дозе 2--4 раза в сутки до прекращения контакта с аллергеном. Препарат можно применять в составе базисной противовоспалительной терапии по 2 разовые дозы 2 раза в сутки на протяжении нескольких месяцев.
В настоящее время для базисной противовоспалительной терапии стали доступны препараты нового класса -- модификаторы лейкотриенов. В медицинской практике уже применяются два антагониста рецепторов лейкотриена D4 -- зафирлукаст (аколат) и монтелукаст (сингулар), а также ингибитор 5-липооксигеназы -- зилетон. Эти препараты обладают противовоспалительным действием, блокируя лейкотриеновую составляющую специфического воспалительного ответа. Наиболее показано назначение этих препаратов больным с обратимой бронхиальной обструкцией, провоцируемой физическим усилием или приемом аспирина и других нестероидных противовоспалительных препаратов. Их также можно применять в комбинации с глюкокортикостероидными гормонами, уменьшая дозу последних.
Глюкокортикостероиды (ГКС), которые вводятся в организм больного различными путями -- ингаляционным, пероральным или инъекционным, являются самыми сильными противовоспалительными средствами. Они возоб- новляют нарушенную чувствительность адренорецепторов бронхов к катехоламинам.
Механизм действия ГКС разносторонний. Основным звеном их действия является влияние на функциональную активность генетического аппарата человеческой клетки. Пассивно проникнув в клетку, гормон связывается с глюкокортикоидным рецептором, находящимся в цитоплазме. Активированный гормонорецепторный комплекс перемещается в ядро клетки и связывается в нем со специальным участком ДНК. "Передвигаясь" по ДНК, указанный комплекс индуцирует работу одних генов и угнетает -- других. Таким образом, осуществляется так называемый геномный эффект ГКС -- способность индуцировать синтез одних и угнетать синтез других белков в клетке. ГКС чаше всего индуцируют синтез липомодулина, который блокирует активность фосфолипазы А2, влияющей на высвобождение арахидоновой кислоты из клеточных мембран. Тем самым уменьшается образование метаболитов арахидоновой кислоты -- лейкотриенов и провоспалительных простагландинов. Существует также негеномный эффект ГКС, который реализуется путем связывания в цитоплазме активированного гормонорецепторного комплекса с нуклеарным фактором капа-В и другими подобными транскрипционными факторами. Следствием указанного эффекта является угнетение различных аспектов воспаления -- образования цитокинов и хемотаксичес- ких факторов, выброс воспалительных ферментов.
Очень важным эффектом глюкокортикостероидной терапии является увеличение количества Р-адренергических рецепторов в бронхах и устранение тахифилаксии (восстановление чувствительности) к Рг-агонистам.
В лечении синдрома бронхиальной обструкции используют различные синтетические ГКС -- гидрокортизон, преднизолон, метилпреднизолон, дексаметазон, триамцинолон, бетаметазон, которые коротким курсом назначают внутрь. Эти препараты существенно отличаются по фармакокинетическим характеристикам и имеют различную эффективность.
Однако системное влияние ГКС вызывает большое количество побочных эффектов -- задержку натрия и воды в организме, потерю калия, остеопороз, миопатию, а также возникновение язвенного поражения желудка или двенадцатиперстной кишки, стероидного сахарного диабета и артериальной гипертензии. Длительное применение этих препаратов приводит к развитию кушингоидного синдрома, подавлению функции надпочечниковых желез, снижению иммунитета к вирусным, бактериальным и грибковым инфекциям, бессоннице и некоторым другим психическим расстройствам. Частота и тяжесть указанных осложнений прямо пропорциональны длительности употребления и величине дозы. Поэтому в базисном противовоспалительном лечении бронхиальной обструкции предпочтение отдают ингаляционным глюкокортикостероидам, которые выпускаются в форме аэрозольного дозирующего ингалятора или сухопорошкового ингалятора.
Ингаляционные ГКС обладают наиболее широким спектром иммуномодулируюших, противовоспалительных и противоаллергических свойств. При ингаляционном пути введения создается высокая терапевтическая концентрация в бронхах при минимуме побочных системных эффектов. Возможность возникновения побочного действия определяется дозой медикаментозного препарата и его биодоступностью. При использовании ингаляционных ГКС в суточной дозе, меньшей 1000 мкг стандартного препарата -- беклометазона, клинические системные побочные эффекты обычно не наблюдаются. Длительное применение ингаляционных ГКС может приводить к местным побочным явлениям: кандидозу слизистой оболочки полости рта и глотки, осиплости голоса или афонии. Лишь тщательное полоскание рта и горла после ингаляции препарата предотвращает возникновение этих осложнений.
В некоторых случаях при наиболее тяжелом течении бронхиальной обструкции ингаляционные ГКС даже в максимальной суточной дозе 2000 мкг (дозировка по беклометазону) оказываются малоэффективными. Тогда дополнительно назначают пероральные ГКС. В случае их длительного применения преимущество отдают преднизолону или метилпреднизолону. Препарат принимают по интермиттирующей схеме в первой половине суток после еды, желательно в дозе, которая не превышает кушингоидную пороговую дозу (10 мг преднизолона или 8 мг метилпреднизолона в сутки).
Улучшение мукоцилиарного клиренса и ликвидация дискринии достигаются, прежде всего, проведением адекватной бронхолитической и противовоспалительной терапии. Восстановление бронхиальной проходимости и уменьшение воспаления слизистой оболочки бронхов создают условия для нормализации секреторной деятельности и улучшения работы мукоцилиарного аппарата. Однако в большинстве случаев желательно назначение мукорегуляторных препаратов или муколитиков -- ацетилцистеина, бромгексина, амброксола.
В основе действия ацетилцистеина лежит разрыв сульфгидрильными группами препарата дисульфидных связей мукополисахаридов бронхиального секрета, способствующий снижению вязкости и улучшению отхождения мокроты. Кроме этого, ацетилцистеин обладает сильными антиоксидантны- ми свойствами. Дополнительный прием жидкости усиливает муколитический эффект препарата. Может назначаться внутрь, а также ингаляционно.
Амброксол нормализует бронхиальную секрецию путем воздействия на секреторные бокаловидные клетки, стимулирует двигательную активность ресничек мерцательного эпителия бронхов, способствует разрежению бронхиального секрета. Препарат активно воздействует на сурфактантную систему легких. Он обусловливает повышение синтеза и секреции сурфактанта, а также препятствует его разрушению под действием неблагоприятных факторов. Применяется внутрь, ингаляционно и парентерально -- внутримышечно и внутривенно. Терапевтический эффект проявляется через 1-2 сут после начала приема препарата. Бромгексин в организме больного превращается в амброксол, обеспечивая вышеизложенные эффекты.
17. Бронхоспастический синдром
Бронхоспастический синдром - симптомокомплекс, развивающийся вследствие сужения просвета мелких бронхов и бронхиол. Симптомы: затруднение дыхания с удлинённым выдохом, повышение тонуса дыхательной мускулатуры, сухие хрипы и цианоз слизистых оболочек. Может возникать при различных заболеваниях органов дыхания как проявление аллергической реакции, при поражении отравляющими веществами, а также как самостоятельное осложнение при хирургических и бронхоскопических вмешательствах. Спазм бронхов сопровождается, как правило, одышкой, затруднением дыхания. Человек не в состоянии откашляться, освободить лёгкие от мокроты. Это связано в первую очередь с резким сужением бронхов и нарушением их проходимости. Совокупность перечисленных признаков, или, как говорят специалисты «бронхоспастический синдром», часто наблюдается при бронхиальной астме, хроническом бронхите, эмфиземе лёгких
18. Клинические симптомы бронхоспастического синдрома
Бронхоспастический синдром проявляется триадой симптомов: приступы удушья экспираторного типа; кашель вначале сухой, удушливый, в конце - с выделением мокроты; распространенные сухие протяжные хрипы, преимущественно на выдохе, слышные на расстоянии.
Варианты течения.
Бронхоспастический синдром гетероаллергического генеза возникает в результате анафилаксии на повторное введение антигена. Может наблюдаться при сывороточной и лекарственной болезни, иногда в ответ на укус насекомых (пчел, ос, шмелей, шершней и др.).
При сывороточной болезни отмечаются отек гортани, высыпание на коже и в зоне инъекции, лихорадка, лимфаденит, артралгии, изредка шок с летальным исходом. Для лекарственной болезни в ряде случаев присущи аллергический ринит, трахеит, бронхит, связь удушья с приемом лекарства, крапивница и другие виды сыпи.
Аутоиммунный бронхоспастический синдром может иметь место при упорном и крайне тяжелом течении СКВ, системной склеродермии, дерматомиозите, узелковом периартериите и других системных васкулитах. Сопровождается лихорадкой, кожными высыпаниями, артралгиями или артритами, лейкоцитозом, эозинофилией и высоким уровнем СОЭ.
Инфекционно-аллергический бронхоспастический синдром при туберкулезе и сифилисе проявляется удушьем на фоне основного заболевания, излечение которого дает стойкую ремиссию. Аллергических заболеваний в семье обычно нет. Мокрота слизисто-гнойная с нейтрофилами. Отсутствуют эозинофилы в крови и мокроте. Введение адреналина не приносит облегчения; прекращение контакта с предполагаемым аллергеном не дает эффекта.
Обтурационный бронхоспастический синдром наблюдается при попадании инородных тел, опухолях и др. При стенозе гортани определяется стридорозное шумное дыхание, охриплость голоса, грубые басовые хрипы в области гортани и трахеи; удушье усиливается в лежачем положении, плохо поддается действию бронхолитиков. Может беспокоить упорный мучительный кашель, который усиливается при перемене положения тела, наблюдается кровохарканье. Мокрота не содержит эозинофилов и спиралей Куршманна. В диагностике помогает бронхологическое и рентгенологическое исследование.
Ирритативный бронхоспастический синдром может наступить при вдыхании пыли, кислот, щелочей, термическом воздействии, отравлении ядохимикатами, боевыми отравляющими веществами и др.
Гемодинамический бронхоспастический синдром возможен при первичной легочно-артериальной гипертензии, тромбозах и эмболиях легочной артерии, венозном застое при пороках сердца. Характеризуется относительной редкостью приступов, застоем и отеком легких, периферическими признаками недостаточности кровообращения, отсутствием эозинофилов в мокроте и крови, эффективностью лечения гликозидами.
Эндокринно-гуморальный бронхоспастический синдром при карциноидном синдроме сопровождается приливами крови к коже лица, шеи, рук; поносами, урчанием в животе; слабостью, головокружением; повышением содержания серотонина в крови. В поздних стадиях развивается стеноз устья легочной артерии и недостаточность трехстворчатого клапана. Вследствие гипопаратиреоидизма возникает склонность мускулатуры к судорожным сокращениям, повышается возбудимость нервной и мышечной системы. Состояние значительно улучшается при введении препаратов кальция.
Бронхоспастический синдром при гипоталамической патологии сопровождается приступами удушья, ознобоподобным дрожанием, повышением температуры тела, частыми позывами на мочеиспускание, длительной адинамией после приступа. БС при болезни Аддисона протекает с потерей массы, пигментацией кожи, большой мышечной слабостью, артериальной гипотензией и успешно лечится глюкокортикоидами.
Бронхоспастический синдром неврогенного генеза может возникнуть после контузий, операций на мозге, при энцефалите, грыже пищеводного отверстия, хроническом холецистите. Характерно наличие вегетативных расстройств, симптомов раздражения вегетативной нервной системы, субфебрилитета. Приступы БС могут быть тяжелыми, а выраженной легочной недостаточности не наблюдается; отсутствуют эозинофилы в крови и мокроте. После холецистэктомии приступы бронхоспастического синдрома исчезают.
Токсический бронхоспастический синдром иногда встречается после приема р-блокаторов, ингибиторов моноаминоксидазы, резерпина, отравления фосфорорганическими соединениями и др.
Симулируя картину бронхиальной астмы, БС может привести к ошибочному диагнозу. Тщательный анализ анамнестических, клинических, лабораторных, рентгенологических данных, а также результатов бронхологического исследования позволяет правильно поставить диагноз и назначить адекватную терапию.
Течение бронхоспастического синдрома
Течение бронхоспастического синдрома различно. Причиной летальных исходов могут быть: асфиксия, острая сердечная недостаточность, паралич дыхательного центра.
19. Классификация бронхоспастического синдрома
Классификация (В. С. Смоленский, И. Г. Даниляк, М. В. Калиничева, 1973)
Жалобы. Больные жалуются на экспираторную одышку, приступы удушья.
Осмотр. Во время приступа бронхоспазма больные принимают вынужденное положение: сидя или стоя с упором на руки. Отмечается цианоз, набухание шейных вен. Грудная клетка расширена, как бы в состоянии постоянного вдоха. Над- и подключичные ямки сглажены, межреберья расширены, дыхательные экскурсии легких ограничены. Дыхание частое, вдох короткий, обычно через рот, выдох удлинен и затруднен.
Перкуссия. Над всей поверхностью легких определяется коробочный перкуторный звук. Наблюдается высокое положение верхушек легких, смещение вниз нижнего края, ограничение его подвижности.
Аускультация. Дыхание ослабленное везикулярное. Часто вообще невозможно определить основной дыхательный шум из-за обилия сухих свистящих хрипов.
Диагностика бронхоспазма. Наиболее характерными признаками являются удлиненный затрудненный выдох, ослабленное дыхание и сухие свистящие хрипы над всей поверхностью легких.
Исследование и диагностика функции внешнего дыхания (ФВД, спирометрия). В частности, проводят определение объема форсированного выдоха за одну секунду (ОФВ1) и жизненной емкости легких (ЖЕЛ). Соотношение этих величин (индекс Тиффно) позволяет судить о степени проходимости бронхов.
- а) исследование исходной ФВД;
- б) ингаляция одной дозы беротека с помощью дозированного карманного ингалятора;
- в) повторное исследование ФВД через 20 мин.
Исследование проводится утром натощак. За 8 часов до исследования отменяются симпатомиметики, за 12 часов -- препараты теофиллина. Изменения показателей бронхиальной проходимости оцениваются относительным приростом спирометрических показателей, который выражается в процентах и
Капнография - капнографы RESPIRONICS (США), WEINMANN (Германия). Капнография позволяет по содержанию углекислого газа в выдыхаемом воздухе оценить глубину дыхания. Этот метод позволяет оценивать изменения глубины дыхания не только в покое, но и при физической нагрузке, а также контролировать эти изменения в процессе выздоровления.
Бронхофонография - компьютерный акустический диагностический комплекс “Паттерн-01”, Россия. Компьютерная бронхофонография - это один из самых современных методов исследования функции дыхания у детей с рождения, чего раньше сделать было просто невозможно. Метод позволяет выявлять нарушения дыхания у детей при спокойном дыхании и даже во сне, помочь в дифференциальной диагностике причин кашля у ребенка - бронхиальная обструкция, избыточное образование мокроты (секрета), затруднение носового дыхания.
Пульсоксиметрия - пульсоксиметры WEINMANN (Германия), MIR (Италия), RESPIRONICS (США). Пульсоксиметрия определяет количество кислорода в крови и частоту пульса, которые изменяются при заболеваниях (гипоксия - недостаток кислорода, учащение пульса) и улучшаются при лечении.
21. Лечение бронхоспастического синдрома
В распоряжении клиницистов имеются средства, предупреждающие выделение биологически активных веществ, образующихся обычно в организме при аллергических реакциях и вызывающих спазм мускулатуры бронхов. Эти препараты, как правило, применяют профилактически. Есть средства, стимулирующие адренорецепторы, что, в свою очередь, вызывает расслабление гладкой мускулатуры бронхов. Их назначают не только для профилактики, но и для купирования уже развившегося спазма бронхов. И наконец, в комплексе лечения брон-хоспастического синдрома используют глюкокортикоиды, способствующие снижению реактивности гладкой мускулатуры бронхов к аллергизирующим факторам. Как видите, каждая группа препаратов имеет свою направленность действия. И потому большую ошибку совершают те, кто принимает тот или иной препарат по совету друзей, знакомых. Самолечение, как правило, не только не приносит больному облегчения, но и может ухудшить состояние, вызвать серьезные осложнения. Назначать лечение должен специалист, учитывая индивидуальные особенности пациента и характер его заболевания.
В последние годы наряду с таблетками, свечами и ампулами широкое распространение получили дозированные аэрозоли бронхорасширяющих препаратов (карманные ингаляторы).
Очень ценно, что препарат, вводимый ингаляционным путем, поступает непосредственно в бронхи и легкие. В связи с этим появилась возможность создавать необходимые терапевтические концентрации лекарства непосредственно в дыхательных путях, а не в крови, что сводит к минимуму побочные реакции со стороны других органов и систем организма. И еще одно положительное свойство аэрозолей-для достижения профилактического и лечебного эффекта требуется малая доза препарата. К тому же из карманных ингаляторов аэрозоль поступает равномерно, чем обеспечивается точность дозировки.
В то же время простота и удобство пользования карманным ингалятором имеют и отрицательные последствия. Нас, врачей, не может не тревожить опасность широкого, а подчас бесконтрольного применения активных бронхорасширяющих средств. Некоторые больные, пренебрегая советами врача, пользуются ингалятором чаще, чем он рекомендовал. А это приводит к передозировке лекарства, что вызывает тяжелые побочные реакции. Поэтому мы бы хотели обратить внимание на то, какой должна быть тактика больного при возникновении у него приступа удушья.
Развившийся приступ следует незамедлительно устранить. Если этого не сделать сразу, вслед за спазмом усиливается процесс образования слизи, что еще больше нарушает проходимость бронхов. Они плотно закупориваются вязкой мокротой. Именно из-за этого иногда так трудно бывает купировать затянувшийся приступ бронхиальной астмы у больного, не принявшего лекарства своевременно. В таких случаях приходится обращаться за неотложной медицинской помощью. Но помимо того, что лекарство надо принять быстро, в самом начале приступа, не менее важно сделать это правильно.
Перед началом ингаляции встряхните баллон, распылитель поднесите ко рту на расстояние 2-3 сантиметров, сделайте полный выдох и одновременно с нажатием на выпускной клапан энергично через рот вдохните аэрозоль. После того, как вы вдохнули лекарство, необходимо возможно дольше задержать выдох. Тогда мельчайшие частицы аэрозоля успеют осесть на слизистой оболочке бронхов и в полной мере проявить свое бронхорасширяющее действие. Как правило, через 20-30 секунд после ингаляции становится легче дышать. Спустя минуту-две вновь вдохните лекарство из ингалятора.
Доза препарата, вводимого в организм за два вдоха, обеспечивает максимальный по силе и продолжительности (примерно 6-8 часов) бронхорасширяющий эффект.
Многочисленные клинические наблюдения показывают, что, если вдыхать аэрозоль более двух раз, эффективность лекарства не увеличится, зато возрастет угроза проявления его побочного действия. О побочном эффекте бронхорасширяющих препаратов свидетельствуют учащение сердцебиения, появление аритмии, сухость во рту, дрожание рук.
Итак, оптимальной терапевтической дозой аэрозоля, обеспечивающей максимальное расширение бронхов и не вызывающей, как правило, побочного действия, является доза, получаемая за два вдоха из карманного ингалятора, снабженного дозирующим клапаном. после ингаляции полезно выпить стакан отвара трав, обладающих отхаркивающим действием (девясил, сосновые почки, чабрец, подорожник, мать-и-мачеха, синюха, корень алтея, солодка, ипекакуана). Отвар готовят на ночь и пьют подогретым.
К препаратам симптоматической терапии относят бронходилятаторы:
- *в2-адреномиметики
- *ксантины
К препаратам базисной терапии относят
- *кромоны
- *ингаляционные глюкокортикостероиды
- *антагонисты лейкотриеновых рецепторов
- *моноклональные антитела
Если не принимать базисную терапию, со временем будет расти потребность в ингаляции бронходилататоров (симптоматических средств). В этом случае и в случае недостаточности дозы базисных препаратов рост потребности в бронходилататорах является признаком неконтролируемого течения заболевания.
К кромонам относят кромогликат натрия (Интал) и недокромил натрия (Тайлед). Эти средства показаны в качестве базисной терапии бронхиальной астмы интермиттирующего и легкого течения. Кромоны уступают по своей эффективности ИГКС. Так как существуют показания для назначения ИГКС уже при легкой степени бронхиальной астмы, кромоны постепенно вытесняются более удобными в использовании ИГКС. Не оправдан также переход на кромоны с ИГКС при условии полного контроля над симптомами минимальными дозами ИГКС.
Глюкокортикостероиды
При астме применяются ингаляционные глюкокортикостероиды, которым не свойственно большинство побочных действиев системных стероидов. При неэффективности ингаляционных кортикостероидов добавляют глюкокортикостероиды для системного применения.
Ингаляционные глюкокортикостероиды (ИГКС)
Ингалятор Беклазон ЭКО
ИГКС -- основная группа препаратов для лечения бронхиальной астмы. Ниже представлена классификация ингаляционных глюкокортикостероидов в зависимости от химической структуры:
Негалогенированные
Будесонид (Пульмикорт, Бенакорт)
Циклесонид (Алвеско)
Хлорированные
Беклометазона дипропионат (Бекотид, Беклоджет, Кленил, Беклазон Эко, Беклазон Эко Легкое Дыхание)
Мометазона фуроат (Асмонекс)
Фторированные
Флунизолид (Ингакорт)
Триамценолона ацетонид
Азмокорт
Флутиказона пропионат (Фликсотид)
Противовоспалительный эффект ИГКС связан с подавлением деятельности клеток воспаления, уменьшением продукции цитокинов, вмешательством в метаболизм арахидоновой кислоты и синтез простагландинов и лейкотриенов, снижением проницаемости сосудов микроциркуляторного русла, предотвращением прямой миграции и активации клеток воспаления, повышением чувствительности b-рецепторов гладкой мускулатуры. ИГКС также увеличивают синтез противовоспалительного белка липокортина-1, путем ингибирования интерлейкина-5 увеличивают апоптоз эозинофилов, тем самым снижая их количество, приводят к стабилизации клеточных мембран. В отличие от системных глюкокортикостероидов, ИГКС липофильны, имеют короткий период полувыведения, быстро инактивируются, обладают местным (топическим) действием, благодаря чему имеют минимальные системные проявления. Наиболее важное свойство -- липофильность, благодаря которому ИГКС накапливаются в дыхательных путях, замедляется их высвобождение из тканей и увеличивается их сродство к глюкокортикоидному рецептору. Легочная биодоступность ИГКС зависит от процента попадания препарата в лёгкие (что определяется типом используемого ингалятора и правильностью техники ингаляции), наличия или отсутствия носителя (лучшие показатели имеют ингаляторы, не содержащие фреон) и от абсорбции препарата в дыхательных путях.
До недавнего времени главенствующией концепцией назначения ИГКС была концепция ступенчатого подхода, что означает что при более тяжелых формах заболевания назначаются более высокие дозы ИГКС.
Комбинации ИГКС и пролонгированных в2-адреномиметиков
Симбикорт Турбухалер
Существуют фиксированные комбинации ИГКС и пролонгированных в2-адреномиметиков, сочетающие в себе средство базисной терапии и симптоматическое средство. Согласно глобальной стратегии GINA, фиксированные комбинации являются наиболее эффективными средствами базисной терапии бронхиальной астмы, так как позволяют снимать приступ и одновременно являются лечебным средством. В России наибольшей популярностью пользуются две такие фиксированные комбинации:
Салметерол + флутиказон (Серетид 25/50, 25/125 и 25/250 мкг/доза, Серетид Мультидиск 50/100, 50/250 и 50/500 мкг/доза)
Формотерол + будесонид (Симбикорт Турбухалер 4,5/80 и 4,5/160 мкг/доза)
Серетид. «Мультидиск»
В состав препарата Серетид входит салметерол в дозе 25 мкг/доза в дозированном аэрозольном ингаляторе и 50 мгк/доза в аппарате «Мультидиск». Максимально-допустимая суточная доза салметерола -- 100 мкг, то есть максимальная кратность применения Серетида составляет 2 вдоха 2 раза для дозированного ингалятора и 1 вдох 2 раза для приспособления «Мультидиск». Это дает Симбикорту преимущество в том случае, если необходимо увеличить дозу ИГКС. Симбикорт содержит формотерол, максимально-допустимая суточная доза которого составляет 24 мкг, делает возможным ингалироваться Симбикортом до 8 раз в сутки. В исследовании SMART выявлен риск, связанный с применением салметерола по сравнению с плацебо. Кроме того, бесспорным преимуществом формотерола является и то, что он начинает действовать сразу после ингаляции, а не через 2 часа, как салметерол.
Патологическое состояние новорожденных, возникающее в первые часы и сутки после рождения вследствие морфофункциональной незрелости легочной ткани и дефицита сурфактанта. Синдром дыхательных расстройств характеризуется дыхательной недостаточностью различной степени выраженности (тахипноэ, цианозом, втяжением уступчивых мест грудной клетки, участием вспомогательной мускулатуры в акте дыхания), признаками угнетения ЦНС и нарушения кровообращения. Синдром дыхательных расстройств диагностируется на основании клинических и рентгенологических данных, оценке показателей зрелости сурфактанта. Лечение синдрома дыхательных расстройств включает оксигенотерапию, инфузионную терапию, антибиотикотерапию, эндотрахеальную инстилляцию сурфактанта.

Общие сведения
Синдром дыхательных расстройств (СДР) – патология раннего неонатального периода, обусловленная структурно-функциональной незрелостью легких и связанным с ней нарушением образования сурфактанта. В зарубежной неонатологии и педиатрии термин «синдром дыхательных расстройств» тождественен понятиям «респираторный дистресс-синдром », «болезнь гиалиновых мембран», «пневмопатии». Синдром дыхательных расстройств развивается примерно у 20% недоношенных (у детей, рожденных ранее 27 недель гестации, – в 82-88% случаев) и 1-2% доношенных новорожденных. Среди причин перинатальной смертности на долю синдрома дыхательных расстройств приходится, по различным данным, от 35 до 75%, что указывает на актуальность и во многом еще нерешенность проблемы выхаживания детей с СДР.
Причины синдрома дыхательных расстройств
Как уже указывалось, патогенез синдрома дыхательных расстройств у новорожденных связан с незрелостью легочной ткани и обусловленной этим недостаточностью антиателектатического фактора - сурфактанта, его неполноценностью, ингибированием или повышенным разрушением.
Сурфактант представляет собой поверхностно-активный липопротеиновый слой, покрывающий альвеолярные клетки и уменьшающий поверхностное натяжение легких, т. е. предупреждающий спадение стенок альвеол. Сурфактант начинает синтезироваться альвеолоцитами с 25-26 недели внутриутробного развития плода, однако его наиболее активное образование происходит с 32-34 недели гестации. Под действием многих факторов, в числе которых гормональная регуляция глюкокортикоидами (кортизолом), катехоламинами (адреналином и норадреналином), эстрогенами, гормонами щитовидной железы, созревание системы сурфактанта завершается к 35-36-й неделе гестации.
Поэтому, чем ниже гестационный возраст новорожденного, тем меньше у него количество сурфактанта в легких. В свою очередь, это приводит к спадению стенок альвеол на выдохе, ателектазу, резкому снижению площади газообмена в легких, развитию гипоксемии, гиперкапнии и респираторного ацидоза. Нарушение альвеолокапиллярной проницаемости приводит к пропотеванию плазмы из капилляров и последующему выпадению гиалиноподобных веществ на поверхность бронхиол и альвеол, что еще в большей степени снижает синтез сурфактанта и способствует развитию ателектазов легких (болезнь гиалиновых мембран). Ацидоз и легочная гипертензия поддерживают сохранение фетальных коммуникаций (открытого овального окна и артериального протока) – это также усугубляет гипоксию, приводит к развитию ДВС-синдрома, отечно-геморрагического синдрома, дальнейшему нарушению образованию сурфактанта.
Риск развития синдрома дыхательных расстройств повышается при недоношенности, морфо-функциональной незрелости по отношению к гестационному возрасту, внутриутробных инфекциях , гипоксии плода и асфиксии новорожденного , ВПС , пороках развития легких , внутричерепных родовых травмах , многоплодии, аспирации мекония и околоплодных вод, врожденном гипотиреозе и др. Материнскими факторами риска развития синдрома дыхательных расстройств у новорожденного могут служить сахарный диабет , анемия, родовое кровотечение , родоразрешение с помощью кесарева сечения.
Классификация синдрома дыхательных расстройств
На основании этиологического принципа различают синдром дыхательных расстройств гипоксического, инфекционного, инфекционно-гипоксического, эндотоксического, генетического (при генетически обусловленной патологии сурфактанта) генеза.
На основании развивающихся патологических сдвигов выделяют 3 степени тяжести синдрома дыхательных расстройств.
I (легкая степень) – возникает у относительно зрелых детей, имеющих при рождении состояние средней тяжести. Симптоматика развивается только при функциональных нагрузках: кормлении, пеленании, проведении манипуляций. ЧД менее 72 в мин.; газовый состав крови не изменен. Состояние новорожденного нормализуется в течение 3-4 дней.
II (средне-тяжелая степень) – ребенок рождается в тяжелом состоянии, которое нередко требует проведения реанимационных мероприятий. Признаки синдрома дыхательных расстройств развиваются в течение 1-2 часов после рождения и сохраняются до 10 суток. Необходимость в дотации кислорода обычно отпадает на 7-8 сутки жизни. На фоне синдрома дыхательных расстройств у каждого второго ребенка возникает пневмония .
III (тяжелая степень) – обычно возникает у незрелых и глубоко недоношенных детей. Признаки синдрома дыхательных расстройств (гипоксия, апноэ, арефлексия, цианоз, резкое угнетение ЦНС, нарушение терморегуляции) возникают с момента рождения. Со стороны сердечно-сосудистой системы отмечается тахикардия или брадикардия , артериальная гипотония , признаки гипоксии миокарда на ЭКГ . Велика вероятность летального исхода.
Симптомы синдрома дыхательных расстройств
Клинические проявления синдрома дыхательных расстройств обычно развиваются на 1-2 сутки жизни новорожденного. Появляется и интенсивно нарастает одышка (ЧД до 60–80 в минуту) с участием в дыхательном акте вспомогательной мускулатуры, втяжением мечевидного отростка грудины и межреберий, раздуванием крыльев носа. Характерны экспираторные шумы («хрюкающий выдох»), обусловленные спазмом голосовой щели, приступы апноэ, синюшность кожных покровов (сначала периоральный и акроцианоз, затем – общий цианоз), пенистые выделения изо рта часто с примесью крови.
У новорожденных с синдромом дыхательных расстройств отмечаются признаки угнетения ЦНС, обусловленные гипоксией, нарастание отека мозга , склонность к внутрижелудочковым кровоизлияниям. ДВС-синдром может проявляться кровоточивостью из мест инъекций, легочным кровотечением и т. д. При тяжелой форме синдрома дыхательных расстройств стремительно развивается острая сердечная недостаточность с гепатомегалией , периферическими отеками.
Другими осложнениями синдрома дыхательных расстройств могут являться пневмонии, пневмоторакс , эмфизема легких , отек легких , ретинопатия недоношенных , некротический энтероколит , почечная недостаточность , сепсис и др. В исходе синдрома дыхательных расстройств у ребенка может отмечаться выздоровление, гиперреактивность бронхов, перинатальная энцефалопатия , нарушения иммунитета, ХНЗЛ (буллезная болезнь, пневмосклероз и др.).
Диагностика синдрома дыхательных расстройств
В клинической практике для оценки степени тяжести синдрома дыхательных расстройств используется шкала И. Сильвермана, где в баллах (от 0 до 2-х) оцениваются следующие критерии: экскурсия грудной клетки, втяжение межреберий на вдохе, западение грудины, раздувание ноздрей, опускание подбородка на вдохе, экспираторные шумы. Суммарная оценка ниже 5 баллов свидетельствует о легкой степени синдрома дыхательных расстройств; выше 5 – средней, 6-9 баллов - о тяжелой и от 10 баллов – о крайне тяжелой степени СДР.
В диагностике синдрома дыхательных расстройств решающее значение отводится рентгенографии легких . Рентгенологическая картина изменяется в различные патогенетические фазы. При рассеянных ателектазах выявляется мозаичная картина, обусловленная чередованием участков снижения пневматизации и вздутия легочной ткани. Для болезни гиалиновых мембран характерны «воздушная бронхограмма», ретикулярно-надозная сетка. В стадии отечно-геморрагического синдрома определяется нечеткость, размытость легочного рисунка, массивные ателектазы, определяющие картину «белого легкого».
Для оценки степени зрелости легочной ткани и системы сурфактанта при синдроме дыхательных расстройств применяется тест, определяющий отношение лецитина к сфингомиелину в околоплодных водах, трахеальном или желудочном аспирате; «пенный» тест с добавлением этанола в анализируемую биологическую жидкость и др. Возможно использование этих же тестов при проведении инвазивной пренатальной диагностики - амниоцентеза , осуществляемого после 32 недели гестации.
Состояние ребенка, обусловленное синдромом дыхательных расстройств, следует отличать от врожденной пневмонии, пороков дыхательной системы, и др.
Ребенок с синдромом дыхательных расстройств нуждается в непрерывном контроле ЧС, ЧД, газового состав крови, КОС; мониторинге показателей общего и биохимического анализа крови, коагулограммы, ЭКГ. Для поддержания оптимальной температуры тела ребенок помещается в кувез, где ему обеспечивается максимальный покой, ИВЛ или ингаляции увлажненного кислорода через носовой катетер, парентеральное питание. Ребенку периодически выполняется трахеальная аспирация, вибрационный и перкуторный массаж грудной клетки .
При синдроме дыхательных расстройств проводится инфузионная терапия раствором глюкозы, гидрокарбоната натрия; трансфузии альбумина и свежезамороженной плазмы; антибиотикотерапия, витаминотерапия, диуретическая терапия. Важным слагаемым профилактики и лечения синдрома дыхательных расстройств является эндотрахеальная инстилляция препаратов сурфактанта.
Прогноз и профилактика синдрома дыхательных расстройств
Последствия синдрома дыхательных расстройств определяются сроком родов, тяжестью дыхательной недостаточности , присоединившимися осложнениями, адекватностью проведения реанимационных и лечебных мероприятий.
В плане профилактики синдрома дыхательных расстройств наиболее важным представляется предупреждение преждевременных родов . В случае угрозы преждевременных родов необходимо проведение терапии, направленной на стимуляцию созревание легочной ткани у плода (дексаметазон, бетаметазон, тироксин, эуфиллин). Недоношенным детям необходимо проводить раннюю (в первые часы после рождения) заместительную терапию сурфактантом.
В дальнейшем дети, перенесшие синдром дыхательных расстройств, кроме участкового педиатра , должны наблюдаться детским неврологом, детским пульмонологом,
1. Синдром очагового уплотнения легочной ткани.
2. Синдром ателектаза легких.
3. Синдром повышенной воздушности легких.
4. Бронхообструктивный синдром.
5. Синдром скопления жидкости в плевральной полости.
6. Синдром скопления воздуха в плевральной полости.
7. Синдром полости в легком.
8. Синдром диссеминированных проце ссов в легочной ткани (с и н д р о м легочной ди сс ем и н ац и и).
9. Синдром дыхательной недостаточности.
Синдром очагового уплотнения легочной ткани.
В его основе лежат 3 группы причин:
заполнение части альвеол воспалительным экссудатом, кровью;
замещение части альвеол соединительной тканью;
прорастание части воздушной ткани легкого опухолью.
Заболевания и состояния, при которых этот синдром выявляется:
1) пневмония; 2) инфаркт-пневмония; 3) туберкулезный инфильтрат; 4) периферический рак легкого; 5) пневмосклероз;6) карнификация.
Жалобы. Одышка (различной степени выраженности в зависимости от распространенности процесса), боль в грудной клетке на стороне поражения (если в патологический процесс вовлечена
плевра или крупный бронх), кровохарканье (“ржавая” мокрота при долевой пневмонии, “малиновое желе” при раке, свежая
кровь при инфаркт-пневмонии); обильное ночное потоотделение, похудание, длительная лихорадка, кашель, кровохарканье при туберкулезе.
Постоянный кашель, не купирующийся лекарствами,~ при раке легкого.
Анамнез заболевания.В анамнезе имеются указания на длительно текущие, повтоРные пневмонии, туберкулез, абсцесс легких.
Объективные симптомы. Их проявления и выраженность зависят от распространенности процесса. Рассмотрим классические проявления синдрома.
Осмотр. Отставание в акте дыхания пораженной половины грудной клетки.
Перкуссия. Притупление перкуторного тона в зоне уплотнения легочной ткани.
Аускультаиия. Три варианта основных дыхательных шумов в зависимости от распространенности очага: 1) бронхиальное дыхание
(большой очаг с хорошей проходимостью вентилирующего бронха); 2) бронховезикулярное дыхание в тех случаях, когда очаги уплотнения перемежаются с воздушной тканью; 3) ослабленное
везикулярное дыхание, когда очаги малы, а вокруг них большие участки нормальной легочной ткани (чаще при небольших
участках пневмосклероза, карнификации, раке легкого).
Побочные дыхательные шумы. 1) консонирующие влажные хрипы - участок уплотнения + наличие жидкого секрета в бронхах;
2) крепитация (пневмония, чаще долевая); 3) шум трения плевры (при вовлечении в патологический процесс плевры, например,
плевропневмония).
Бронхофония. Усиление над очагом поражения.
Рентгенологическое исследование. Очаг затенения в легочной ткани (ее уплотнение).
Классическим примером типичных симптомов при синдроме уплотнения (консолидации) легочной ткани, выявляемых при физикальном исследовании над зоной поражения, является долевая
пневмония в разгар заболевания: при пальпации - усиление голосового дрожания, при перкуссии - тупой перкуторный звук,
при аускультации - бронхиальное дыхание и крепитация, усиление бронхофонии.
Синдром ателектаза легких.
Ателектаз (гр. ateles - несовершившийся, неполный + ektasis- растягивание) - патологическое состояние легкого или его части, при котором легочные альвеолы не содержат воздуха или
содержат его в уменьшенном количестве и представляются спавшимися.
Выделяют полный и неполный ателектаз (дистелектаз).
Общепринятой классификации ателектазов не существует.
В зависимости от механизма возникновения выделяют 3 основных варианта ателектаза:
обтурационный;
компрессионный (сдавление ткани легкого);
дистензионный, или функциональный (нарушение условий растяжения легких на вдохе: слабость дыхательных мышц, особенно
диафрагмы, угнетение дыхательного центра).
Выделяют также рефлекторный ателектаз (активное сокращение элементов легкого). Так, при длительных хирургических операциях
иногда наблюдается полное спадение легкого или обоих легких при полной проходимости бронхиального дерева.
Обтурационный ателектаз. Причина обтурационного ателектаза — нарушение проходимости бронхов в результате закупорки или сдавления снаружи опухолью, рубцами, лимфоузлами.
Жалобы. Одышка, сердцебиение, цианоз. Цианоз обусловлен сбросом (шунтирование) неоксигенированной крови из малого
круга в большой круг кровообращения.
Осмотр: а) грудная клетка на стороне ателектаза западает; б) отстает в акте дыхания; в) межреберные промежутки сужены.
Пальпация. Резистентность грудной клетки снижена, голосово дрожание ослаблено.
перкуссия. Сравнительная - над зоной ателектаза звук укорочен или тупой (все зависит от степени абсорбции воздуха). При полной закупорке бронха полное поглощение О2 из альвеоляр-
01 о воздуха происходит в течение 30 мин, СО2 - через 2 ч, азота в течение 6 — 8 ч.
Топографическая. Отмечается смещение границ сердца и средостения в целом в сторону ателектаза. Особенно это заметно при массивном правостороннем ателектазе, когда сердеч
ный толчок может смещаться вправо от грудины.
Аускультация. Резкое ослабление или полное отсутствие везикулярного дыхания, бронхофония ослаблена.
Рентгенологические данные: а) межреберья сужены; б) срединная тень смещена в сторону ателектаза; в) в области ателектаза — гомогенная тень; г) высокое расположение купола диафрагмы и
подциафрагмальных органов; д) вздутие неизмененных отделов легких (викарная эмфизема).
Компрессионный ателектаз развивается в результате внешнего сдавления легочной ткани, обусловленного:
1) скоплением жидкости в плевральной полости;
2) объемными процессами средостения, перикарда, пищевода, лимфоузлов;
3) скоплением газа в плевральной полости;
4) опухолями плевры;
5) аневризмой аорты.
Жалобы обусловлены основным заболеванием.
Осмотр. Отставание грудной клетки на стороне ателектаза при дыхании. Однако западения грудной клетки и сужения меж- реберных промежутков не наблюдается.
Пальпация. В зоне ателектаза — усиление голосового дрожания, в зоне скопления жидкости или газа - ослабление.
Перкуссия. Сравнительная - притупление перкуторного тона.
Зона притупления чаще определяется основным патологическим процессом (жидкостью, опухолью и т. д.). Если легкое прижимается к корню, то перкуторный звук становится притупленно-
тимпаническим.
Топографическая - органы средостения смещены, как правило, в здоровую сторону, снижение подвижности нижнего легочного края.
Аускультация. Ослабленное бронхиальное дыхание, у с и л е н н а я бронхофония над зоной ателектаза.
Синдром повышенной воздушности легких.
Синдром, который обусловлен патологическим р а с ш и р е н и е м воздушных пространств дистальнее терминальных бронхиол. Это патологическое расширение воздушных пространств н а зы в а е т с я эмфиземой легких.
Бронхообструктивный синдром.
Нарушение бронхиальной проходимости происходит в результате воспаления слизистой оболочки бронхов, ее отека; скопления
в просвете бронхов избыточного количества секрета с измененными реологическими свойствами; спазма гладкой мускулатуры бронхов.
Бронхообструктивный синдром полиэтиологичен и встречается при ряде заболеваний, но наиболее часто - при хронической обструктивной болезни легких и бронхиальной астме. Часто
бронхообструктивный синдром сочетается с эмфиземой.
Жалобы на затрудненное дыхание (одышку), больше выраженное на выдохе (экспираторное диспноэ). Часто выявляются “свистящее” дыхание, дистанционные хрипы; приступы удушья,
характерные для бронхиальной астмы.
Осмотр. Вынужденное положение - ортопноэ (при приступе бронхиальной астмы); участие вспомогательной мускулатуры в
акте дыхания; грудная клетка в положении вдоха (приподнята); дистанционные хрипы.
Пальпация. При сопутствующей эмфиземе усилена ригидность грудной клетки и ослаблено голосовое дрожание.
Перкуссия. При наличии сопутствующей эмфиземы - коробочный звук, опущены нижние границы и другие признаки повышенной воздушности легких.
Аускультация: 1) жесткое дыхание (шероховатое, грубое дыхание, сохраняющее черты везикулярного, т. к. в целом сохранена длительность дыхательных фаз); 2) жесткое дыхание с удлиненным
выдохом; выдох выслушивается на протяжении всего цикла или занимает большую его часть; 3) сухие свистящие хрипы как характерный признак поражения мелких бронхов (бронхоспазм +
наличие вязкого секрета).
Рентгенография. Усиление и деформация легочного рисунка. функция внешнего дыхания.
Синдром скопления жидкости в плевральной полости.
Этот синдром является полиэтиологическим. Наиболее частые варианты синдрома:
Гидроторакс - скопление невоспалительной жидкости при СН
экссудативный плеврит (туберкулез, пневмония, рак легких, |оПухоль плевры и др.);
■ гемоторакс (скопление крови) - при травмах грудной клетки;
хилоторакс - скопление лимфы в плевральной полости.
Жалобы зависят от основного заболевания. При значительном скоплении жидкости - одышка, цианоз, сердцебиение.
Осмотр. Выбухание половины грудной клетки на стороне скопления жидкости; отставание ее при дыхании; сглаженность кмежреберных промежутков.
Пальпация: 1) резистентность грудной клетки увеличена на стороне поражения. Кожная складка там же более “толстая”, чем на противоположной стороне (симптом Винтриха); 2) голосовое
дрожание ослаблено или полностью отсутствует.
Перкуссия. Сравнительная перкуссия: тупой или притупленный перкуторный звук в зависимости от объема жидкости. В зоне максимального скопления жидкости перкуссия выявляет абсолютную тупость. В зонах, где слой жидкости тоньше, определяется притупление перкуторного тона.
Считают, что свободный плевральный выпот может быть определен с помощью перкуссии, если его объем превышает 300- 500 мл. Повышение его уровня на 500 мл соответствует увеличению зоны притупления перкуторного звука на одно ребро кверху (например, увеличение зоны притупления с V по IV ребро свидетельствует
об увеличении количества свободной жидкости в плевральной полости на 500 мл).
Топографическая перкуссия. Притупление перкуторного тона имеет дугообразную границу, максимально возвышающуюся по задней подмышечной линии (линия Дамуазо-Франклина, Соко- лова-Эллиса-Дамуазо). Затем эта линия спускается кпереди косо вниз.
Синдром скопления воздуха в плевральной полости.
Пневмоторакс - патологическое состояние, которое развивается в результате появления сообщения бронхов с плевральной полостью, т. е. в тех случаях, когда происходит разрыв легочной
ткани и висцеральной плевры, что приводит к поступлению воздуха в плевральную полость.
Различают следующие виды пневмоторакса: и
искусственный (для лечения больных туберкулезом);
травматический;
спонтанный (когда разрыв легочной ткани происходит в результате наличия врожденных булл, эмфизематозных в здутий, абсцесса легкого, спаек легких и т. д.).
Вы деляют также пневмоторакс: 1) открытый, 2) закрытый, 3) клапанный.
Синдром полости в легком.
Причинами образования полости в легких служит ряд заболеваний:
1) острый и хронический абсцесс легкого; 2) туберкулез легких; 3) распад опухоли легкого; 4) бронхоэктазы; 5) кисты легких.
Жалобы больного зависят от характера заболевания. Классические физикальные симптомы полости появляются в тех случаях,
когда полость: 1) свободна от содержимого, 2) сообщена сбронхом, 3) достаточно крупная.
Осмотр. Отставание в акте дыхания больной половины грудной клетки.
Пальпаиия. Усиление голосового дрожания.
Перкуссия. Притупленно-тимпанический звук (полость, как правило, образуется в зоне уплотнения легочной ткани или окружена валом воспаления). При наличии поверхностно расположенной
крупной полости - тимпанит высокий или низкий в зависимости от состояния стенок полости.
Металлический перкуторный тон образуется в полостях, имеющих не менее 6 см в диаметре и гладкие стенки. Уменьшение экскурсии нижнего легочного края пораженного легкого.
Аускультация. Бронхиальное дыхание с амфорическим оттенком (амфорическое дыхание). Бронхофония усилена.
Рентгенологически. Участок просветления с уровнем жидкости.
Синдром диссеминированных процессов в легочной ткани
Синдром легочных диссеминаций объединяет большую группу различных заболеваний, объединенных 2 основными п р о я в л е ниями:
прогрессирующей одышкой и характерными рентгенологическими изменениями в легких.
Синдром дыхательной недостаточности.
Различают 3 степени хронической дыхательной недостаточности:
I с т е п е н ь - появление одышки при выполнении умеренной физической нагрузки или нагрузок, превышающих повседневные;
II с т е п е н ь - появление одышки при выполнении незначительных физических нагрузок (или при повседневных нагрузках);
III с т е п е н ь - появление одышки в покое.
Нарушение внешнего дыхания происходит при нарушении:
а) вентиляции в результате обструктивных или рестриктивных нарушений; б) процессов диффузии в результате структурноморфологических изменений альвеолярно-капиллярной мембраны
(фиброзирующие альвеолиты, эмфизема и др.); в) перфузии легких кровью в результате тромбоза или эмболии легочных сосудов, или поражения сосудистой стенки (тромбоэмболия ветвей
легочной артерии, легочные ангииты при системных заболеваниях соединительной ткани и др.).
Дыхательная и легочная недостаточность - неравнозначные понятия. Легочная недостаточность подразумевает изменения только аппарата внешнего дыхания, а дыхательная - изменения
всех 3 этапов дыхания (вентиляции, транспорта газов кровью и газообмена в тканях). Но чаще всего причиной дыхательной недостаточности является легочная недостаточность.
Внелегочные причины дыхательной недостаточности:
нарушения центральной регуляции дыхания;
нарушения нейромышечной передачи импульса;
поражения дыхательных мышц;
поражения грудной клетки (деформации, травмы и др.);
болезни системы крови;
болезни системы кровообращения.
Легочные причины дыхательной недостаточности:
обструкция дыхательных путей;
рестрикция альвеолярной ткани;
утолщение альвеолярно-капиллярной мембраны (фиброз, отек и т. д.);
поражение легочных капилляров.




